
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
恒瑞医药
600276 |
0.72%
|
最新:57.6
开盘:57.13 昨收:57.19 |
开盘%:-0.1%
振幅%:2.92% 换手%:1.42% |
最高:58.28
最低:56.61 量比:1.75 |
总市值:3823 亿
流通值:3674 亿 成交额:64 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
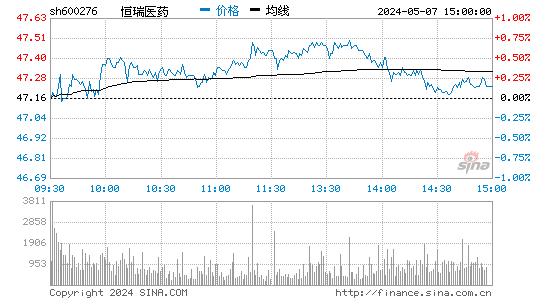
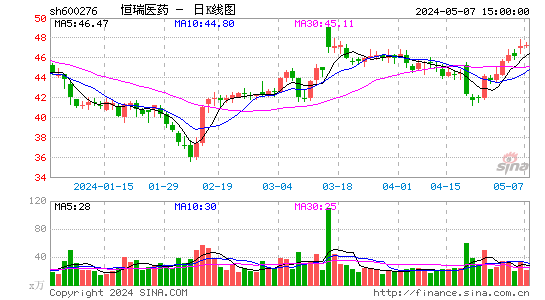
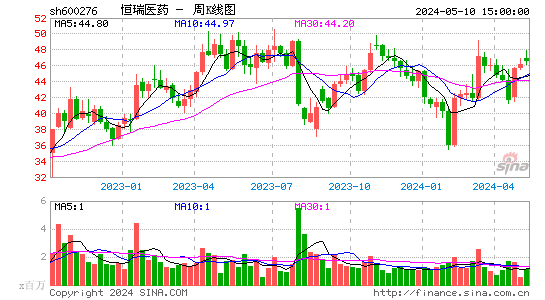
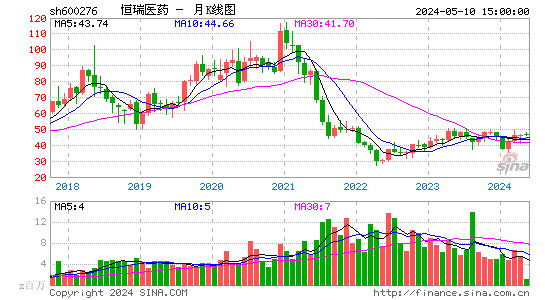
恒瑞医药股票概览
了解恒瑞医药及其股票投资价值
公司概况
恒瑞医药是一家专注于医药创新和高质量发展的公司,致力于提供优质的医药产品和服务。公司拥有强大的研发团队和先进的技术平台,不断推动医药领域的创新和发展。
业务领域
研发创新:恒瑞医药在抗肿瘤、麻醉、抗感染等多个领域拥有领先的产品线,并持续投入研发,拓展新的治疗领域。
市场营销:公司拥有完善的营销网络和专业的销售团队,能够迅速将创新产品推向市场,满足患者需求。
国际合作:恒瑞医药积极拓展国际市场,与国际知名药企开展合作,提升公司的全球竞争力。
财务表现
近年来,恒瑞医药的财务表现稳健。公司营收持续增长,净利润水平保持在较高水平。同时,公司的研发投入也在不断增加,为公司的长期发展提供了有力保障。
股票投资价值
作为医药行业的佼佼者,恒瑞医药的股票具有较高的投资价值。公司的创新能力和稳健的财务表现使其成为众多投资者的优选。然而,股票投资存在风险,投资者需结合自身风险承受能力进行决策。
总结
恒瑞医药是一家具有创新精神和稳健财务表现的医药公司。其业务领域广泛,研发实力强大,股票具有较高的投资价值。关键词:恒瑞医药、股票、投资价值。
以上是对恒瑞医药及其股票的全面介绍,希望能够帮助投资者更好地了解这家公司和其股票的投资价值。
2025-07-09 16:09
【香港恒生指数收跌1.06% 巨星传奇涨超90%】7月9日电,香港恒生指数收跌1.06%,恒生科技指数跌1.76%。巨星传奇涨超94%,恒瑞医药涨超15%;金涌投资跌超44%,国泰君安国际跌超5%,华虹半导体跌超4%,阿里巴巴跌超3%。
2025-07-09 15:10
【7月9日资金流向】主力净流入行业板块前五:大金融,银行,传媒,信托,游戏;主力净流入概念板块前五:虚拟数字人,AIGC概念,多模态,大消费,IP经济/谷子经济;主力净流入个股前十:恒瑞医药、中油资本、宁德时代、中文在线、华工科技、康美药业、中国移动、中国联通、跨境通、工业富联
2025-07-09 15:06
【沪深两市今日成交额合计1.51万亿元,宁德时代成交额居首】7月9日,沪深两市成交额合计1.51万亿元,较上一交易日放量约512.38亿元。其中,沪市成交额5959.63亿元,深市成交额9092.24亿元。宁德时代成交额居首,为79.48亿元。其后是东方财富、中油资本、工业富联、恒瑞医药,成交额分别为78.35亿元、72.59亿元、70.99亿元、65.08亿元。
2025-07-09 14:19
【主力资金监控:电子板块净流出超65亿】7月9日电,星矿数据显示,今日主力资金净流入文化传媒、商贸零售、出版等板块,净流出电子、有色金属、电新行业等板块,其中电子板块净流出超65亿元。个股方面,跨境通涨停,主力资金净买入8.09亿元位居首位,恒瑞医药、中文在线、巨力索具主力资金净流入居前;中油资本遭净卖出超5亿元位居首位,东方财富、北方铜业、紫金矿业主力资金净流出额居前。
2025-07-09 13:11
【恒瑞医药港股午后拉升涨超14%】恒瑞医药港股午后拉升涨超14%,A股涨幅扩大至5%。
2025-07-09 11:33
【国家发改委秘书长袁达:截至2024年我国累计在研创新药达4000余款】7月9日电,7月9日,国家发展改革委秘书长袁达在国新办发布会上表示,截至2024年,我国累计在研的创新药达到4000余款,约占全球的30%。
2025-07-09 10:20
【创新药概念股持续反弹,九芝堂触及涨停】创新药概念股持续反弹,九芝堂触及涨停,普蕊斯涨超15%,美迪西、科兴制药、恒瑞医药纷纷上扬。
2025-07-08 21:06
【公告精选:圣农发展上半年净利同比预增732.89%—830.88%;大洋电机筹划发行H股并在香港联交所上市】7月8日电,【经营数据】圣农发展:2025年上半年净利同比预增732.89%—830.88%深深房A:上半年净利同比预增1411.7%—2034.17%豪鹏科技:2025年上半年净利同比预增228.03%—271.77%大金重工:2025年上半年净利同比预增193.32%—227.83%巨化股份:上半年净利同比预增136%到155%捷顺科技:2025年上半年净利同比预增105.68%—193.82%汇中股份:2025年上半年净利同比预增95%—105%亚太股份:2025年上半年净利同比预增81.97%—101.13%塔牌集团:2025年上半年净利同比预增80%—100%金诚信:上半年净利同比预增74.62%到82.78%凯龙股份:2025年上半年净利同比预增53.64%—84.37%朗博科技:上半年净利同比预增49.51%到66.12%圣泉集团:上半年净利同比预增48.19%到54.83%海陆重工:2025年上半年净利同比预增48.92%—60.68%越秀资本:2025年上半年净利同比预增45%—55%华工科技:2025年上半年净利同比预增42.43%—52.03%鼎龙股份:2025年上半年净利同比预增33.12%—46.9%华测导航:2025年上半年净利同比预增27.37%—33.34%海大集团:2025年上半年净利同比预增17.64%—31.76%云铝股份:2025年上半年净利同比预增7.19%—11.16%尚纬股份:上半年预亏2700万元到3500万元金证股份:预计上半年亏损3235.9万元至4622.71万元唐人神:6月生猪销售收入6.98亿元 同比上升26%天康生物:6月份生猪销售收入3.42亿元 同比下降19.53%京基智农:6月生猪销售收入3.1亿元克明食品:控股子公司6月生猪销售收入同比增长111.22%晓鸣股份:6月鸡产品销售收入9676.33万元 同比增长182.52%立华股份:6月肉鸡销售收入9.42亿元 同比下降21.3%山钢股份:预计上半年实现利润总额2.93亿元【热点】6天5板华银电力:近6个交易日公司股票累计换手率为80.95% 显著高于同行业上市公司平均水平5天3板欣灵电气:近期公司经营情况及内外部经营环境未发生重大变化四连板森林包装:截至目前公司消费类包装业务占比较小4天3板新亚电子:公司“藕芯结构”技术应用产品所产生的营收占比较小三连板新中港:公司主营业务未发生重大变化2连板永安期货:不存在应披露而未披露的重大信息二连板渝开发:不存在未披露重大事项二连板金时科技:公司未开展任何与稳定币概念相关的业务四方新材:7月7日和7月8日 公司董事、高级管理人员谢涛、江洪波合计减持8万股金橙子:2024年激光3D打印控制系统相关产品收入占公司总体收入比例不足2%大智慧:公司日常经营情况正常 不存在重大变化永太科技:公司“一种双氟磺酰亚胺锂的制备方法”专利尚在有效期内大洋电机:筹划发行H股并在香港联交所上市【并购重组】光韵达:拟3.52亿元收购亿联无限56.0299%股权正帆科技:拟收购汉京半导体62.23%股权【增减持、回购】硕贝德:拟2000万元至3000万元回购股份严牌股份:控股股东一致行动人拟增持1700万元至3400万元公司股份海信家电:控股股东一致行动人拟增持692.81万股至1385.62万股公司股份埃夫特:股东拟合计减持不超5%公司股份朗特智能:控股股东一致行动人拟减持公司不超3%股份真爱美家:控股股东之一致行动人拟减持不超3%公司股份东方中科:大连金投拟减持公司不超3%股份新通联:股东毕方投资拟减持不超3%公司股份星网宇达:实控人拟减持不超3%公司股份超图软件:实控人及部分董监高拟减持不超2.01%公司股份金域医学:国创开元拟减持不超1%公司股份吉祥航空:东航产投拟减持不超1%公司股份元祖股份:兰馨成长及其一致行动人拟减持公司不超1%股份【中标合同】安徽建工:联合体中标S27呼和浩特至鄂尔多斯高速公路(呼和浩特段)项目赛象科技:中标5.33亿元空客天津飞机大部件运输工装夹具项目通达股份:中标1.8亿元南方电网项目普利特:孙公司签署钠离子电池储能系统采购合同继峰股份:全资子公司获得乘用车座椅总成项目定点【重大投资】卓越新能:拟7亿元投建泰国生物能源项目乖宝宠物:拟6.5亿元投建智能仓储及数智化分拣中心项目大富科技:拟不超过1亿元投资安徽云塔菲菱科思:拟使用部分超募资金投建光通信传输系统设备之接入网设备项目海通发展:拟使用不超6500万美元购置干散货船舶【其他】八亿时空:开展边缘计算业务弘元绿能:子公司签署《合作经营协议》太极实业:控股子公司海太半导体与SK海力士完成了四期合同的正式签署上纬新材:控股股东筹划控制权变更事项取得进展 股票复牌新朋股份:全资子公司参投基金的投资项目上市豫能控股:豫能台前2×1000MW煤电项目获得核准盟升电子:5名股东拟询价转让3.68%公司股份江苏国信:子公司国信沙洲一台100万千瓦机组投产大金重工:波罗的海地区某海上风电场全部单桩产品到港交付完毕甬金股份:公司实际控制人取保候审中色股份:控股子公司取得新采矿许可证伟创电气:取得专利证书和软件著作权证书宏川智慧:下属公司成为大商所纯苯指定交割仓库上海莱士:“SR604注射液”进入Ⅱb期临床试验研究泰恩康:子公司盐酸毛果芸香碱滴眼液注册上市获受理舒泰神:取得STSA-1002注射液的Ib/II期临床研究总结报告鲁抗医药:吉非替尼片获药品注册证书恒瑞医药:子公司获得药物临床试验批准通知书仟源医药:子公司依巴斯汀原料药获批上市
2025-07-08 17:18
【恒瑞医药:子公司HRS-9821吸入粉雾剂用于慢性阻塞性肺疾病临床试验获批】恒瑞医药7月8日公告,公司子公司广东恒瑞医药有限公司收到国家药品监督管理局核准签发关于HRS-9821吸入粉雾剂的《药物临床试验批准通知书》,同意本品开展用于慢性阻塞性肺疾病(COPD)的临床试验。
2025-07-08 16:14
【恒瑞医药:子公司获得HRS-9821吸入粉雾剂临床试验批准通知书】7月8日电,恒瑞医药(600276.SH)公告称,子公司广东恒瑞医药有限公司收到国家药监局核准签发的HRS-9821吸入粉雾剂的《药物临床试验批准通知书》,同意开展用于慢性阻塞性肺疾病(COPD)的临床试验。HRS-9821是小分子PDE3/PDE4抑制剂,可有效抑制呼吸道炎症、扩张支气管,临床拟用于COPD的维持治疗。截至目前,该项目累计研发投入约3,843万元。根据相关法律法规,该药物在获得临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2025-07-03 16:59
【恒瑞医药:子公司全氟己基辛烷滴眼液获得药品注册证书】恒瑞医药7月3日公告,公司子公司成都盛迪医药有限公司获得国家药品监督管理局核准签发的全氟己基辛烷滴眼液《药品注册证书》。本品用于治疗睑板腺功能障碍相关干眼。
2025-07-03 16:56
【恒瑞医药:子公司收到SHR-4506注射液临床试验批准通知书】7月3日电,恒瑞医药(600276.SH)公告称,子公司苏州盛迪亚生物医药有限公司收到国家药监局核准签发关于SHR-4506注射液的《药物临床试验批准通知书》,将于近期开展临床试验。SHR-4506注射液是公司自主研发的1类治疗用生物制品,拟用于治疗晚期恶性肿瘤,目前国内外尚无同类药物获批上市。
2025-07-02 14:47
【摩根士丹利:给予恒瑞医药增持评级 目标价78港元】7月2日电,摩根士丹利今日就恒瑞医药(01276.HK)发布研报称,该公司在内地药企中拥有最广泛且最平衡的产品组合及管线,公司预期2025至2027年将有47款新药获批上市,预计恒瑞2024至2027年间创新药销售的年均复合增长率为34%。给予目标价78港元,首予“增持”评级。
2025-07-02 07:25
【6月以来获融资净买入额居前的创新药概念股出炉】7月2日电,今年以来,中国创新药产业迎来多项突破性进展。从多款创新药集中获批上市,到企业在国际学术舞台展示亮眼临床数据、出海交易金额屡创新高,行业活力尽显。业内人士认为,目前中国创新药进入成果兑现阶段,研发进展催化较多,有望持续成为2025年医药板块投资主线。二级市场表现方面,据证券时报·数据宝统计,截至7月1日收盘,年内Wind创新药指数上涨超26%,创新药概念股今年以来平均上涨35%,大幅跑赢同期上证指数。舒泰神、益方生物-U、三生国健、泰恩康、荣昌生物、科兴制药年内涨幅均超100%。资金面上,据数据宝统计,6月以来融资净买入超1亿元的创新药概念股有15只。博瑞医药、恒瑞医药、康龙化成、特宝生物、贝达药业等获融资净买入额排在前五位。
2025-07-01 12:46
【创新药重磅消息 融资资金出手加仓股揭晓】7月1日电,国家医保局、国家卫生健康委印发《支持创新药高质量发展的若干措施》(简称《若干措施》)。《若干措施》坚持以人民健康为中心的发展理念,聚焦我国创新药发展面临的突出问题,立足医保、卫生健康部门职能,提出5方面16条措施,对创新药研发、准入、入院使用和多元支付进行全链条支持,实现“真支持创新、支持真创新、支持差异化创新”目标。《若干措施》的出台将对创新药产业高质量发展发挥重要作用。二级市场表现方面,据数据宝统计,截至6月30日收盘,创新药概念股今年以来平均上涨30.28%,大幅跑赢同期上证指数。资金面上,数据宝统计,6月以来获融资净买入超1亿元的创新药概念股有15只。博瑞医药、恒瑞医药、康龙化成、特宝生物、贝达药业等融资净买入额排在前五位。
2025-06-30 16:37
恒瑞医药:布比卡因脂质体注射液获得药品注册批准。
2025-06-27 16:14
恒瑞医药:获得HRS-8829注射用浓溶液药物临床试验批准通知书
2025-06-20 20:54
【公告精选:海南华铁称公司不涉及稳定币业务;光庭信息拟投建智能网联汽车数字汽车创新实验室项目】6月20日电,【热点】海南华铁:公司不涉及稳定币业务 未与蚂蚁数科就RWA达成协议绿通科技:美国低速载人车辆“双反”终裁对公司在美业务存在较大影响四连板诺德股份:铜箔业务应用于固态电池领域的收入占总营业收入不足1%三连板长城军工:股价短期涨幅较大 后续股票可能存在较大下跌风险二连板海科新源:近期公司经营情况及内外部经营环境未发生重大变化江龙船艇:公司经营情况、内外部经营环境未发生重大变化天岳先进:香港联交所上市委员会已审阅公司H股上市申请凌云光:参股公司长光辰芯向香港联交所递交上市申请奥普光电:参股公司长光辰芯向香港联交所递交上市申请【并购重组】杰美特:拟收购思腾合力控制权 预计构成重大资产重组应流股份:拟4.84亿元收购控股子公司应流航空28.46%股权渝三峡A:拟通过收购及增资方式取得蔚蓝时代控制权神开股份:拟6000万元收购蓝海智信51%股权桐昆股份:拟以154.27万元收购中灿能源100%股权【再融资】长缆科技:拟定增募资不超4.6亿元 用于高压超高压电缆附件产能扩充等项目神开股份:拟定增募资不超2.2亿元 用于高端海洋工程装备制造基地项目【股权变动】锦江酒店:拟转让锦江食品、锦箸餐饮100%股权天永智能:拟1568万元出售江苏天永49%股权【增减持、回购】腾讯控股6月20日耗资约5亿港元回购99.7万股股份南威软件:实控人拟减持不超2%公司股份广东明珠:股东拟减持不超1.5%公司股份阿拉丁:晶真文化拟减持不超0.72%公司股份渝三峡A:近日出售北陆药业299.88万股 增加净利润约1225万元【经营数据】宁波华翔:因欧洲业务剥离 上半年预计亏损2.73亿元—3.69亿元中国电建:前五月境外签约合同金额同比增长30.51%中国建筑:前五月新签合同总额18412亿元 同比增长1.7%【中标合同】浙江交科:下属公司联合预中标18.97亿元国道改建工程国晟科技:二级控股子公司签订约10.43亿元日常经营重大合同华康洁净:联合预中标4.75亿元医院配套工程【重大投资】中国银行:拟向中银欧洲增资3亿欧元吉电股份:拟49.2亿元投建梨树绿色甲醇创新示范项目巨化股份:控股子公司甘肃巨化出资8亿元增资其全资子公司巨化新能源神农集团:拟投资5.5亿元建设龙门猪场等3个项目光庭信息:拟投建智能网联汽车数字汽车创新实验室项目赛轮轮胎:赛轮新加坡拟投资500万澳元认购MTS信托11.09%份额亚盛集团:全资子公司拟出资3000万元设立公司 加强供应链建设汉仪股份:拟设立控股子公司 布局IP嵌入游戏步长制药:控股子公司山东步长传方拟对外投资400万元设立子公司【其他】康缘药业:肖伟辞去董事长职务军信股份:与长沙数字集团有限公司签署战略合作协议北玻股份:全资子公司与博远机电签署战略合作协议 开展工业领域节能改造业务耀皮玻璃:大连耀皮浮法玻璃生产线将于6月23日起停产实施升级改造张小泉:法院裁定受理控股股东重整申请粤宏远A:终止重大资产重组事项任子行:公司股票自6月24日起被实施其他风险警示科德教育:公司控制权变更事项终止松井股份:湖南三迪拟进行增资扩股引入战略投资者新疆浩源:6月23日起公司证券简称变更为“万憬能源”恒瑞医药:多款药品获药物临床试验批准康希诺:13价肺炎球菌多糖结合疫苗获药品注册证书智飞生物:子公司吸附破伤风疫苗临床试验获批泰恩康:子公司收到药品注册受理通知书汇宇制药:注射用HY0001a获得药物临床试验批准常山药业:艾本那肽注射液用于减重适应症的临床试验申请获批国药现代:注射用头孢唑肟钠通过仿制药一致性评价昂利康:子公司通过药品GMP符合性检查九州通:地塞米松磷酸钠注射液获药品注册证书
2025-06-20 16:15
【恒瑞医药:收到6个药物临床试验批准通知书】6月20日电,恒瑞医药(600276.SH)公告称,公司及子公司收到国家药监局核准签发关于SHR2554片、注射用SHR-A1811等6个药物的《药物临床试验批准通知书》,将于近期开展临床试验。这些药物包括新型口服EZH2抑制剂SHR2554片、靶向HER2的抗体药物偶联物注射用SHR-A1811、靶向Nectin-4的抗体药物偶联物注射用SHR-A2102、人源化抗PD-L1单克隆抗体阿得贝利单抗注射液、靶向Claudin18.2的抗体药物偶联物注射用SHR-A1904以及抗PD-L1/TGF-βRII双功能融合蛋白SHR-1701注射液。这些项目累计研发投入分别为SHR2554片约1.8亿元,注射用SHR-A1811约11.7亿元,注射用SHR-A2102约2.05亿元,阿得贝利单抗注射液约8.87亿元,注射用SHR-A1904约1.43亿元,SHR-1701注射液约6.74亿元。
2025-06-20 09:22
【港股开盘:恒生指数涨0.23%,恒生科技指数涨0.3%,低价油气股多数高开】6月20日,港股开盘,恒生指数高开0.23%,恒生科技指数高开0.30%。低价油气股多数高开,吉星新能源涨近8%。恒瑞医药涨近2%,被调入港股通标的证券名单。泡泡玛特跌超6%,消息面上,泡泡玛特Labubu大量补货后二手报价腰斩。
2025-06-20 08:49
【深交所:将恒瑞医药调入港股通标的证券名单】6月20日电,深交所公告,港股通标的证券名单发生调整并自2025年06月20日起生效,调入恒瑞医药。
2025-06-18 10:23
【6月17日7股获杠杆资金加仓超亿元】6月18日电,截至6月17日,市场融资余额合计1.82万亿元,较前一交易日增加52.71亿元。个股方面,6月17日共7股获融资净买入超亿元,中国平安融资净买入额居首,当日净买入3.16亿元,其次是恒瑞医药、新易盛,融资净买入金额分别为1.96亿元、1.53亿元,融资净买入金额居前的还有寒武纪、海联金汇、中国太保、光线传媒等。
2025-06-17 14:21
【主力资金监控:光线传媒净卖出超9亿】6月17日电,星矿数据显示,今日主力资金净流入航运港口、交通运输、能源金属等板块,净流出文化传媒、医药、计算机等板块,其中文化传媒板块净流出超43亿元。个股方面,融发核电涨停,主力资金净买入5.11亿元位居首位,立讯精密、贝因美、招商南油主力资金净流入居前;光线传媒遭净卖出超9亿元位居首位,恒瑞医药、恒生电子、元隆雅图主力资金净流出额居前。
2025-06-17 06:15
【深化对外开放合作,上交所组织上市公司赴欧洲推介交流】为进一步完善对外开放格局、便利跨境资本投融资合作,上交所近日组织沪市优质上市公司代表赴英国伦敦和瑞士日内瓦,开展资本市场推介与国际交流活动。此次活动通过公司集中路演、机构一对一拜访等形式深入交流、促进理解,全面展示中国资本市场的开放成果与发展潜力。 参加本次推介的恒瑞医药、万华化学、小商品城、宁波港、中信金属、中国铝业、中国中车、中国中免、中远海控、东方电缆、金山办公、九号公司等12家沪市公司,分别来自生物医药、高端制造、水上运输、信息技术、商务服务等行业,均是所属领域的领军企业。(上证报)
2025-06-16 13:30
【高盛再次唱多:全球资金回归中国 看好中国“十巨头”股票】6月16日电,高盛首席中国股票策略师刘劲津近日发布名为《中国民营企业的回归:潮流已经逆转》的研究报告。刘劲津指出,在各种宏观、政策和微观因素驱动下,中国民营企业的中期投资前景正在改善。高盛还仿效美股“七巨头”,列出了中国“十巨头”,即高盛特别看好的十大中国民营上市公司。他们分别是:腾讯、阿里巴巴、小米、比亚迪、美团、网易、美的、恒瑞医药、携程和安踏。上述十家公司的总市值达1.6万亿美元,占MSCI中国指数权重的42%,日交易额达110亿美元。高盛分析师预计,未来两年“十巨头”的盈利将增长13%(复合年增长率),市盈率为16倍。“十巨头”将共同体现中国人工智能/科技发展、“走出去”、新消费以及提高股东回报等最新经济主题。此外,刘劲津特别指出,投资民营企业并不意味着排斥国有企业——高盛重申,其仍偏好于“高质量”的中国国有企业和股东回报组合。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 股市实战策略:精准换股,制胜之道
- 智慧换股:解锁股市盈利新策略
- 期货购买指南:全面解析期货交易入门与风险防控
- 投资大师的智慧:面对股市跌市的三大黄金策略
- 股票看盘深度解析:掌握关键技巧,洞悉市场动向
- 期货保证金算法全解析:理解交易安全阀的关键
- 弱市中的智慧生存:投资者自保策略与机遇探索
- 箱体震荡与真假突破的奥秘:精准捕捉企稳信号
- 尾盘成交量变化揭秘:投资者如何洞悉股市先机
- 揭秘股价翻番股的四大黄金法则
- 揭秘“三榜提名”炒股绝技,精准捕捉黑马股
- 透视破净股:机遇与挑战并存的投资迷局
- 如何利用底部十字星捕捉即将爆发的牛股
- 买卖盘:观察主力动向的重要窗口
- 散户投资炒股:避开亏钱陷阱,解锁盈利之道
- 散户如何识破主力洗盘策略,稳守牛股斩获收益
- 股市智慧:掌握买卖时机,稳健投资之道
- 炒股十大禁忌:避免常见错误,稳健投资之道
- 打板艺术:解锁A股短线交易的盈利密码
- 揭秘股市上涨奥秘:多维度分析股票后期上涨潜力
当前版本:V3.0

 VIP复盘网
VIP复盘网
