
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
奥赛康
002755 |
3.46%
|
最新:28.4
开盘:27.67 昨收:27.45 |
开盘%:0.8%
振幅%:6.27% 换手%:2.11% |
最高:29
最低:27.28 量比:1.06 |
总市值:264 亿
流通值:264 亿 成交额:9 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
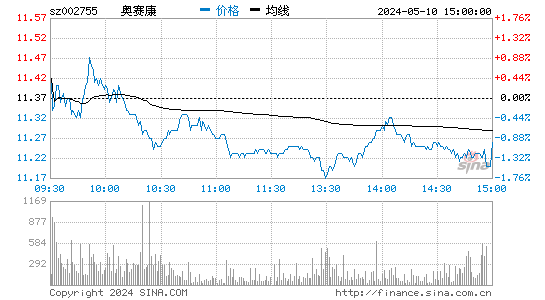
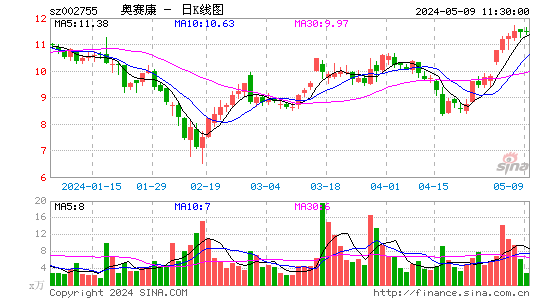
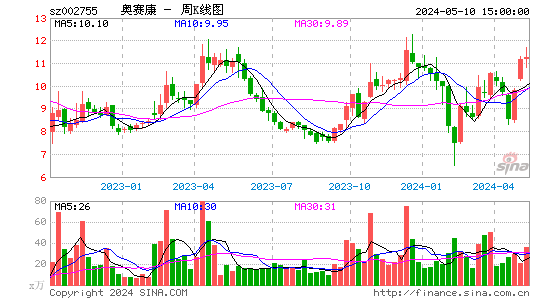
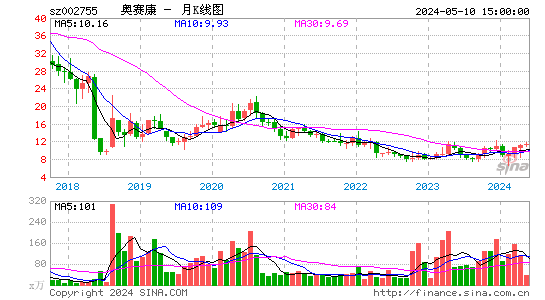
奥赛康股票概况
从公司概况到财务表现的全面解析
公司概况
奥赛康,股票代码002755,是一家专注于医药制造业的公司,主要产品涉及消化、肿瘤、耐药感染、慢性病等四大治疗领域。公司在南京设有多个生产基地,并拥有完整的研发、生产、销售体系。
财务表现
奥赛康近年来财务表现稳健。根据最新财务报告,公司总市值达到一定规模,每股收益(TTM)持续增长,显示出良好的盈利能力。同时,公司的流动比率和速动比率均保持在较高水平,表明其拥有较强的流动性。
产品线
奥赛康的产品线丰富,涵盖了多个治疗领域。其中,公司在抗消化性溃疡质子泵抑制剂(PPI)注射剂产品细分市场中占有领先地位,为该细分领域的龙头企业。
市场地位
奥赛康在中国医药细分市场中具有较高的品牌影响力。公司通过整合内外部资源建立了完整的市场销售体系,主要采用经销商模式开展产品销售,并积极参与各省的药品集中采购招投标。
总结:
奥赛康作为一家专注于医药制造业的公司,凭借丰富的产品线、稳健的财务表现和较高的市场地位,在行业内具有显著优势。未来,公司有望继续保持增长态势,为投资者带来稳定回报。
2025-07-29 20:35
【奥赛康:股东拟减持不超过1.5%公司股份】7月29日电,奥赛康(002755.SZ)公告称,公司计划在公告披露之日起15个交易日后的连续90个自然日内,以集中竞价和大宗交易方式减持公司股份不超过13,922,400股,不超过公司总股本的1.5%。减持原因是股东经营发展需要。减持期间为2025年8月20日至2025年11月17日。减持方式包括集中竞价和大宗交易。若减持期间公司有除权除息事项,减持数量将相应调整。
2025-07-04 13:11
创新药概念股涨势扩大,广生堂、热景生物均20cm涨停,塞力医疗、海正药业、奥赛康等多股封板,神州细胞、汇宇制药涨超10%。
2025-06-23 20:26
【公告精选:皖仪科技拟联合建立和运作“核聚变关键真空测量设备研发联合实验室”】6月23日电,【热点】兴业股份:半导体光刻胶用酚醛树脂目前仅处于送样测试阶段,暂不对业绩产生影响。嘉澳环保:因涉嫌信息披露违法违规,证监会决定对公司立案。五连板诺德股份:公司铜箔业务应用于固态电池领域收入占总营收不足1%。捷强装备:公司股票交易严重异常波动,存在市场情绪过热的情形。二连板英联股份:经营情况、内外部经营环境未发生重大变化。【增减持】博闻科技:上海德朋拟减持公司不超3%股份。上海洗霸:控股股东及其一致行动人拟减持公司不超3%股份。中国黄金:中信证券投资拟减持公司不超0.83%股份。九强生物:股东中国医药投资有限公司拟不低于3000万元增持公司股份。云天励飞:股东拟合计减持公司不超3%股份。五矿新能:股东深圳安晏拟减持公司不超3%股份。石头科技:实控人自愿承诺12个月内不减持公司股份。中晶科技:实控人拟减持公司不超过2%股份。【回购】浪潮信息:拟2亿元—3亿元回购股份。日联科技:拟1000万元至2000万元回购股份。寒武纪:将回购价格上限上调为不超过818.87元/股。【合同中标】皖仪科技:与能源研究院签署《联合实验室共建协议》,双方决定联合建立和运作“核聚变关键真空测量设备研发联合实验室”。珠海冠宇:获东风日产定点为其开发和供应汽车低压锂电池。金智科技:公司及子公司近日合计中标1.13亿元项目。崧盛股份:拟与重庆精刚传动针对“机器人谐波减速器及智能关节技术开发应用”进行技术开发合作。【重大投资】桂冠电力:拟约3.95亿元投建马田光伏项目。天佑德酒:子公司拟1.6亿元投建酒庄改扩建项目。广州港:子公司拟投建广州港南沙港区五期工程项目,总投资概算145亿元。【并购重组】华升股份:拟购买易信科技100%股份,股票明起复牌。国投中鲁:筹划重大资产重组,股票明起停牌,拟向国投集团等相关方发行股份购买中国电子工程设计院股份有限公司(简称“电子院”)控股权。海联讯:换股吸收合并杭汽轮事项申请获深交所受理。*ST星光:终止“造价通”平台资产收购事项。红棉股份:拟收购亚洲食品股权,进一步扩大饮料板块业务规模。天亿马:拟收购星云开物100%股权,股票复牌。【再融资】冠昊生物:终止向特定对象发行股票事项并撤回申请文件。倍杰特:拟定增募资不超10亿元,用于供水保障能力提升工程等项目。【其他】泰凌微:端侧AI新品2025年二季度销售额达千万元规模。奥赛康:利厄替尼片III期临床研究结果在《柳叶刀·呼吸病学》发布。晶科能源:182N型高效单晶硅电池及N型TOPCon高效光伏组件转化效率获第三方认证,全面积电池转换效率达到27.02%,创造了大面积N型单晶钝化接触(TOPCon)电池转换效率新的纪录。长安汽车:控股股东名称变更为“辰致汽车科技集团有限公司”。三花智控:公司发行H股股票于6月23日在香港联交所上市。
2025-06-23 17:34
【奥赛康:利厄替尼片III期临床研究结果在《柳叶刀·呼吸病学》发布】6月23日电,奥赛康(002755)6月23日晚间公告,公司一类创新药利厄替尼片(奥壹新®)近日在国际医学期刊《柳叶刀·呼吸病学》(IF:32.8)发布该产品的III期临床研究结果。利厄替尼片是第三代表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI),用于具有EGFR突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的一线、二线治疗。
2025-06-22 16:28
【奥赛康:子公司甲氨蝶呤注射液获得药品注册证书】奥赛康6月22日公告,全资子公司江苏奥赛康药业有限公司于近日收到国家药品监督管理局核准签发的甲氨蝶呤注射液《药品注册证书》。甲氨蝶呤是一种二氢叶酸还原酶抑制剂类药物,可干扰DNA合成、修复和细胞复制,具有广谱抗肿瘤活性,可单独使用治疗乳腺癌、妊娠性绒毛膜癌等,或与其它化疗药物联合使用治疗成骨肉瘤、急性白血病等,大剂量单独应用或与其它化疗药物联合应用治疗成骨肉瘤、急性白血病、支气管肺癌或头颈部表皮癌,以及用于银屑病化疗。
2025-06-13 09:41
创新药概念反复活跃,百洋医药涨超10%,舒泰神涨超8%,振东制药、奥赛康、睿智医药、翰宇药业等跟涨。
2025-06-12 14:46
【创新药概念震荡反弹,海思科、奥赛康双双涨停】创新药概念震荡反弹,海思科、奥赛康双双涨停,荣昌生物、舒泰神、睿智医药、益方生物-U等跟涨。
2025-06-12 13:20
【创新药概念再度拉升 百济神州涨超7%创历史新高】6月12日电,午后创新药概念再度拉升,百济神州涨超7%,再创历史新高,此前奥赛康涨停,荣昌生物、睿智医药、博瑞医药涨超10%,海思科、舒泰神、万邦德等多股涨超5%。消息面上,今日记者获悉,港股创新药企中国生物制药在第46届高盛全球医疗健康年会上透露,今年将至少有1个重量级的out-license交易落地。该股受此消息刺激大涨超15%,总市值突破1000亿港元。
2025-06-12 13:15
创新药概念午后拉升,奥赛康涨停,博瑞医药、睿智医药涨超10%,海思科、长春高新、微芯生物、舒泰神等涨幅居前
2025-04-25 20:27
奥赛康:子公司利厄替尼片一线治疗适应症上市申请获得批准
2025-03-07 21:31
【国家发展改革委副主任李春临同志主持召开民营企业座谈会】2月27日,国家发展改革委副主任李春临同志在江苏省南京市主持召开民营企业座谈会。江苏润和软件股份有限公司、亿嘉和科技股份有限公司、南京埃斯顿酷卓科技股份有限公司、江苏芯德半导体科技股份有限公司、江苏满运软件科技有限公司、江苏奥赛康药业有限公司、南京翼辉信息技术有限公司、南京世和基因生物技术股份有限公司负责人围绕企业发展情况、存在的困难问题和有关工作建议作了交流发言。会议指出,下一步,国家发展改革委将持续深化与民营企业的沟通交流,积极回应企业关切和诉求,进一步提升政策制定的精准性和前瞻性,为民营企业做强做优做大创造有利外部环境。(国家发改委微信公号)
2025-03-07 21:31
【国家发展改革委副主任李春临同志主持召开民营企业座谈会】2月27日,国家发展改革委副主任李春临同志在江苏省南京市主持召开民营企业座谈会。江苏润和软件股份有限公司、亿嘉和科技股份有限公司、南京埃斯顿酷卓科技股份有限公司、江苏芯德半导体科技股份有限公司、江苏满运软件科技有限公司、江苏奥赛康药业有限公司、南京翼辉信息技术有限公司、南京世和基因生物技术股份有限公司负责人围绕企业发展情况、存在的困难问题和有关工作建议作了交流发言。会议指出,下一步,国家发展改革委将持续深化与民营企业的沟通交流,积极回应企业关切和诉求,进一步提升政策制定的精准性和前瞻性,为民营企业做强做优做大创造有利外部环境。(国家发改委微信公号)
2025-02-10 17:18
奥赛康:子公司硫酸艾沙康唑胶囊获得药品注册上市许可申请受理通知书
2025-01-24 07:57
【奥赛康:子公司在2025年ASCO GI发布创新药ASKB589治疗一线晚期胃癌研究成果】奥赛康公告,本项研究中,ASKB589(靶向 CLDN18.2 单克隆抗体)联合 CAPOX(奥沙利铂及卡培他滨)以及 PD-1 抑制剂作为一线治疗方案,表现出显著的肿瘤缓解,且显示出持续的生存获益、良好的耐受性,联合 PD-1 抑制剂给药并未观察到额外的安全性风险。本研究结果支持开展以 CLDN18.2 中高表达的 IV 期胃/胃食管交界处腺癌患者为目标人群的 ASKB589 三联疗法 III 期临床研究。本次公布的研究成果是 ASKB589 联合化疗及 PD-1 抑制剂治疗一线晚期胃癌的最新疗效数据,为探索全新的一线标准治疗提供了新的循证医学支持,有望填补当前治疗领域的空白。目前,ASKB589 联合化疗及 PD-1 抑制剂的 III 期临床研究正在开展中。
2025-01-20 18:40
奥赛康:子公司曲氟尿苷替匹嘧啶片获得药品注册证书
2025-01-20 10:11
【创新药板块大幅反弹 药明康德等多股涨超5%】1月20日电,奥赛康涨停,药明康德、荣昌生物、神州细胞、百济神州、海创药业、百利天恒等多股涨超5%。消息面上,1月17日,国家医疗保障局举行新闻发布会。国家医疗保障局医药服务管理司司长黄心宇介绍,2025年我国将出台丙类药品目录,该目录将纳入超出“保基本”功能定位、暂时无法纳入基本医保药品目录的创新药品品种。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 精准捕捉强势股低吸时机:策略与技巧深度剖析
- KDJ指标深度解析:精准捕捉市场波动的利器
- 炒股为何频陷亏损泥潭:揭秘背后真相
- 揭秘股市强势板块持续性之谜
- 股票买入策略:上涨买还是下跌买?
- 炒股智慧:四静箴言引领股市风雨路
- 股票卖出后大涨的应对策略:从心态到技巧的全方位解析
- 套利与套期保值:策略差异与市场智慧的深度剖析
- 股市怎么复盘最有效
- 绩优股建仓策略与炒作艺术深度剖析
- 股市智慧:深入解析“形意三十六决”
- 深度解析KDJ指标:运用技巧与注意事项
- 揭秘股市奇才的选股策略:趋势、技巧与心态的三重奏
- 菜鸟到操盘大师的蜕变之旅
- 掌握股市智慧:五策略破解“一买就跌,一卖就涨”魔咒
- 选股策略:五大关键条件助你挑选优质股票
- 股市实战指南:精准把握买卖时机
- 股市见底先兆:深度解析市场反转信号
- 股票解套策略:掌握换股的九大黄金法则
- MACD策略精解:掌握“三把斧”,稳健获利十二年
当前版本:V3.0

 VIP复盘网
VIP复盘网
