
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
科伦药业
002422 |
-1.1%
|
最新:37.78
开盘:38.01 昨收:38.2 |
开盘%:-0.5%
振幅%:2.72% 换手%:1.36% |
最高:38.44
最低:37.4 量比:0.83 |
总市值:604 亿
流通值:493 亿 成交额:13 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
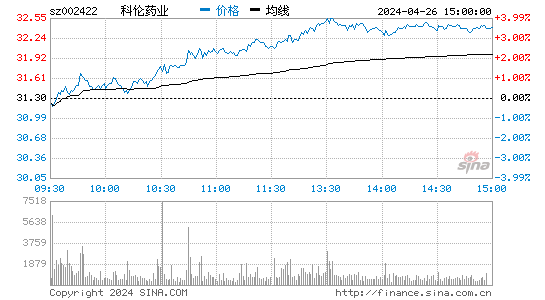
- 分时图
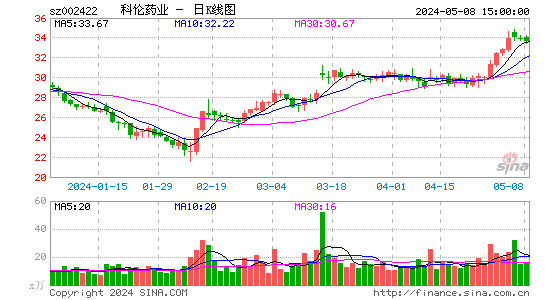
- 日K图
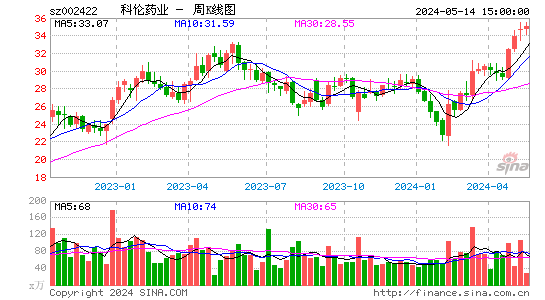
- 周K图
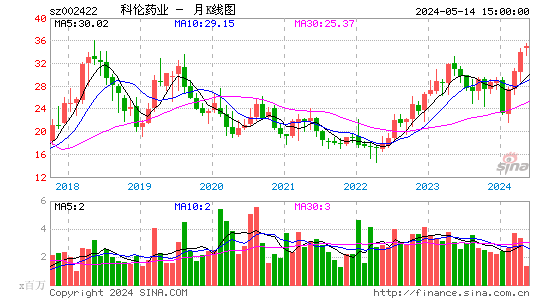
- 月K图
科伦药业股票概况
全面了解科伦药业及其股市表现
公司概况
科伦药业是中国知名的药业公司之一,致力于药品的研发、生产和销售。公司拥有先进的生产设备和严格的质量控制体系,确保药品的安全性和有效性。其产品线涵盖了多个治疗领域,满足了广大患者的需求。
业务布局
研发创新:科伦药业注重研发创新,投入大量资源进行新药研发,不断提升自身的研发实力和技术水平。
市场拓展:公司在国内外市场均有布局,通过多样化的销售策略和渠道拓展,实现了业务的快速增长。
供应链管理:科伦药业拥有完善的供应链管理体系,确保原材料的供应和产品的高效流通。
股市表现
科伦药业的股票在股市中表现稳定,吸引了众多投资者的关注。其股价波动受公司业绩、市场环境和政策影响,但整体呈现上涨趋势。
总结
科伦药业作为一家具有实力的药业公司,在股市中具有较高的人气。随着公司业务的不断拓展和研发实力的提升,其未来发展前景广阔。
{summary}
科伦药业作为药业领域的佼佼者,在研发创新、市场拓展和供应链管理方面均表现出色。其股票在股市中表现稳定,未来发展潜力巨大,值得投资者关注。{/summary}
2025-06-12 18:27
【科伦药业:注射用头孢唑林钠/氯化钠注射液获得药品注册批准】6月12日电,科伦药业(002422.SZ)公告称,公司子公司湖南科伦制药有限公司的化学药品“注射用头孢唑林钠/氯化钠注射液”于近日获得国家药品监督管理局的药品注册批准。该药品为粉液双室袋包装形式,适用于紧急状态下的快速救治,可有效避免配制过程中的错配和污染风险。头孢唑林钠是抗感染治疗的经典用药,目前临床广泛用于各种手术围术期预防用药和治疗敏感菌所致的感染。该药品为国家医保乙类品种,2024年头孢唑林钠注射剂中国销售13.5亿元。科伦药业的注射用头孢唑林钠/氯化钠注射液为国内第2家获批粉液双室袋包装形式。
2025-06-11 08:36
【科伦药业:子公司核心产品获国家药品监督管理局突破性疗法认定】6月11日电,科伦药业(002422)6月11日早间公告,公司近日获悉,公司控股子公司科伦博泰靶向人滋养细胞表面抗原2(TROP2)的抗体偶联药物(ADC)芦康沙妥珠单抗(sac-TMT)(佳泰莱®)联合抗程序性细胞死亡配体1(PD-L1)单克隆抗体塔戈利单抗(科泰莱®)一线治疗无驱动基因突变的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)获中国国家药品监督管理局(NMPA)药品评审中心(CDE)授予突破性疗法认定。作为科伦博泰的核心产品,芦康沙妥珠单抗(sac-TMT)是一款科伦博泰拥有自主知识产权的新型TROP2 ADC,针对 NSCLC、BC、胃癌(GC)、妇科肿瘤等晚期实体瘤。塔戈利单抗是全球首个获批用于一线治疗鼻咽癌的PD-L1单克隆抗体。
2025-06-11 08:10
科伦药业:子公司核心产品TROP2 ADC芦康沙妥珠单抗(sac-TMT)联合PD-L1单抗塔戈利单抗一线治疗无驱动基因突变的局部晚期或转移性非鳞状非小细胞肺癌获国家药品监督管理局突破性疗法认定。
2025-06-06 18:17
【科伦药业回应饶毅炮轰麦角硫因系“假药”:产品定位为“非药品”】6月5日,北京大学校务委员会副主任、理学部主任饶毅直指科伦药业旗下的麦角硫因胶囊为“假药”,并引发关注。在饶毅发文后,6月6日,科伦药业回应,称二者的核心观点差异,在于麦角硫因胶囊究竟是膳食补充剂还是药品。科伦药业方面表示,麦角硫因的定位是健康管理工具,是国际上公认的膳食补充剂,“而非药品,又何来‘假药’一说”。并称,“(饶毅)文中‘未获药品批准即属无效’的论断有点武断和对膳食补充剂存有偏见”。(每经)
2025-06-05 12:11
【科伦药业:控股子公司科伦博泰拟配股净筹19.43亿港元】6月5日电,科伦药业(002422)6月5日午间公告,公司近日获悉公司控股子公司科伦博泰根据其股东大会的发行股份的一般性授权,于6月5日与2名配售代理订立配售协议。根据协议约定,配售代理同意促使向不少于6名承配人配售591.8万股科伦博泰H股股份,配售价格331.8港元/股,此次配售的完成取决于配售协议约定的若干先决条件的达成。此次配售所得款项净额预计为19.43亿港元,将用于科伦博泰的产品研发、临床试验、注册备案、制造及商业化;提升内部研发技术能力、加强外部合作及拓展产品管线组合;补充营运资金及作一般企业用途。
2025-06-05 11:19
【饶毅称麦角硫因是“假药” 科伦药业:不便置评他人言论】6月5日电,饶毅在公众号用“肌肉男真人‘赤膊上阵’”、“大肆推广麦角硫因”等措辞以及视频部分截图影射科伦药业董事长代言公司麦角硫因产品一事,并直言麦角硫因就是“假药”,文章还称,“对于顾客来说,吃麦角硫因只能证明自己容易受骗”。对此,科伦药业证券部工作人员对以投资者身份致电的记者回应称,“我们没有关注到(该公众号文章内容)。对于其他人的评论,我们也不方便做公开评论,取决于您自己通过各方面综合信息的判断。”小财注:上月,科伦药业董事长刘革新亲自赤裸上半身为公司麦角硫因产品代言,引发社会热议,A股抗衰老概念股大涨。(记者 何凡)
2025-05-23 17:00
科伦药业:子公司根据SKB378/HBM9378/WIN378的独占性许可协议收到现金及股权支付的首付款。
2025-05-23 13:42
创新药概念股持续走高,信立泰、科伦药业双双创历史新高,阳光诺和冲击20CM涨停,众生药业此前涨停,海辰药业、贝达药业、泓博医药涨超10%,舒泰神、海翔药业、泰格医药、华海药业等多股涨超5%。
2025-05-23 08:03
【科伦药业:子公司将在2025年美国临床肿瘤学会年会上公布六项创新药物研究成果】科伦药业公告,公司控股子公司科伦博泰将于 2025 年 5 月 30 日至 6 月 3 日期间在美国伊利诺伊州芝加哥市举行的 2025 年美国临床肿瘤学会(ASCO)年会上公布六项由科伦博泰主导的临床研究成果,包括其抗人滋养细胞表面抗原 2(TROP2)的抗体偶联药物(ADC)芦康沙妥珠单抗(sac-TMT)(佳泰莱®)、抗程序性细胞死亡配体 1(PD-L1)单克隆抗体塔戈利单抗(tagitanlimab)(科泰莱®)以及转染过程中重排(RET)抑制剂 KL590586(A400/EP0031)的相关数据。
2025-05-22 08:33
【科伦药业:子公司核心产品芦康沙妥珠单抗(sac-TMT)的新增适应症上市申请(sNDA)获国家药品监督管理局受理】科伦药业公告,公司控股子公司科伦博泰靶向人滋养细胞表面抗原 2(TROP2)的抗体偶联药物(ADC)芦康沙妥珠单抗(sac-TMT,亦称SKB264/MK-2870)(佳泰莱®)的一项新增适应症上市申请已获中国国家药品监督管理局(NMPA)药品审评中心(CDE)受理,用于治疗既往接受过内分泌治疗且在晚期或转移性阶段接受过其他系统治疗的不可切除的局部晚期或转移性激素受体阳性(HR+)且人表皮生长因子受体 2 阴性(HER2-)乳腺癌(BC)成人患者。本次受理是基于 OptiTROP-Breast02 注册 3 期研究的积极结果。该申请是芦康沙妥珠单抗(sac-TMT)获 NMPA 受理的第四个适应症上市申请。
2025-05-21 20:26
【科伦药业:子公司注射用比阿培南/氯化钠注射液获得药品注册批准】5月21日电,科伦药业(002422.SZ)公告称,公司子公司湖南科伦制药有限公司的化学药品“注射用比阿培南/氯化钠注射液”已获得国家药品监督管理局的药品注册批准。该药品为国内首家获批的粉液双室袋包装形式,具有抗菌谱广、对β-内酰胺酶稳定、抗菌活性强等特点,且肾毒性和中枢神经系统毒性更低。
2025-05-20 09:31
创新药概念盘初拉升,华海药业直线涨停,舒泰神、益方生物涨超7%,亿帆医药、凯因科技、科伦药业等跟涨
2025-05-15 15:48
【5月15日连板股分析:资金继续抱团高位股 麦角硫因概念异军突起】今日共50股涨停,连板股总数20只,其中三连板及以上个股11只,上一交易日共17只连板股,连板股晋级率64.70%(不含ST股、退市股)。个股方面,全市场超3800只个股下跌,短线资金继续抱团高位股,渝三峡A走出12天8板,股价创近8年来新高,尤夫股份晋级3连板,近18个交易日录得9次涨停。不过值得注意的是,国芳集团、襄阳轴承等部分高位股午后跳水,或表明资金对高位股分歧加大。板块方面,麦角硫因概念异军突起,川宁生物、拓新药业20CM涨停,金达威、丽人丽妆、福瑞达涨停,并带动合成生物、食用菌等相关细分上涨,消息面上,科伦药业董事长刘革新赤膊上阵,展示健硕肌肉,为旗下抗衰老产品“麦角硫因胶囊”代言引发热议。
2025-05-15 15:35
【今日投资舆情热点】 1)麦角硫因、医美:科伦药业一则麦角硫因胶囊广告引发热议,公司董事长刘革新亲自上阵担任产品代言人。 2)港口航运:美线运价开始上涨,部分船公司已经上调5月下半月美线运价,部分南美船只调往美线。 3)纺织服装:5月12日关税下调当晚,库存量几近见底的美国客户开始疯狂下单,希望抓住90天的出货窗口期。 4)工业母机:工信部召开座谈会,聚焦加快推动工业母机产业高质量发展,避免“内卷式”竞争、同质化发展。
2025-05-15 10:18
创新药板块探底拉升,哈三联涨停,万邦医药涨超10%,九芝堂、科伦药业、凯莱英等跟涨
2025-05-15 09:59
【合成生物概念逆势拉升 川宁生物20CM涨停】 5月15日电,川宁生物20CM涨停,芭薇股份涨近20%创历史新高,拓新药业、无锡晶海、美邦科技、福瑞达等涨幅靠前。消息面上,近日,科伦药业一则麦角硫因胶囊广告引发热议,公司董事长刘革新亲自上阵担任产品代言人。有业内人士告诉记者,麦角硫因由生物提取,现在也可通过合成生物学方式来生产,具有抗氧化、细胞保护等功效。
2025-04-30 13:12
创新药概念持续活跃,百济神州、诺诚健华、锦波生物均创出历史新高,科伦药业、益方生物、泽璟制药、华东医药、恒瑞医药等涨幅靠前
2025-04-21 18:40
科伦药业:子公司创新ADC药物SKB518新药临床试验申请获美国食品药品监督管理局批准
2025-04-01 15:29
【4月1日资金流向】主力净流入行业板块前五:医药,创新药,化学原料药,体外诊断,信托; 主力净流入概念板块前五:健康中国,核聚变,军工集团,PD-1抑制剂,央企改革; 主力净流入个股前十:恒瑞医药、中航产融、寒武纪、江淮汽车、红宝丽、阳光电源、科伦药业、旭光电子、鲁抗医药、中国核建
2025-03-25 19:51
科伦药业:子公司放射性核素偶联药物(RDC)SKB107新药临床试验申请获国家药品监督管理局批准
2025-03-10 19:19
科伦药业:子公司核心产品芦康沙妥珠单抗(sac-TMT)获国家药品监督管理局批准第二个适应症(用于EGFR突变非小细胞肺癌治疗)上市
2025-03-10 19:16
【科伦药业:子公司核心产品芦康沙妥珠单抗(sac-TMT)获批第二个适应症】3月10日电,科伦药业(002422.SZ)公告称,公司控股子公司科伦博泰的靶向人滋养细胞表面抗原2(TROP2)的抗体药物偶联物(ADC)芦康沙妥珠单抗(sac-TMT)获国家药品监督管理局批准第二个适应症,用于治疗经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)和含铂化疗治疗后进展的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)成人患者。这是全球首个在肺癌适应症获批上市的TROP2 ADC药物。该批准基于一项多中心、随机、对照关键临床研究,结果显示芦康沙妥珠单抗在客观缓解率(ORR)、无进展生存期(PFS)和总生存期(OS)方面显著优于多西他赛。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 精准捕捉个股卖点:K线图与移动平均线的智慧交融
- 短线操作的雷区:新手必知的八大禁忌
- 揭秘涨停股的“瞄准器”:异动K线与九阳真经
- 短线交易的艺术:洞悉市场,精准出击
- 潜伏以待,智取股市:中小散户的选股与潜伏策略
- 大盘与个股:投资策略的智慧抉择
- 揭秘股市奥秘:精准定位个股底部策略
- 主力试盘策略深度剖析:揭秘市场操控的艺术
- 洞察股市龙头奥秘,精准捕捉市场脉搏
- 精准捕捉优质成长股:选股策略与时机把握
- 全球视野下的A股“慢牛”格局解析
- 揭秘均线交易法则:五三买卖策略实战解析
- 股市盈利秘籍:揭秘四种典型交易者及其成功之道
- 透视股市庄家策略:揭秘下影线背后的市场转折信号
- 揭秘消费股内在价值:从吉列到中国消费品企业的成长之路
- 股市风云:深入剖析六种量价关系及其策略应用
- 揭秘股市神秘信号:精准捕捉揉搓线起涨点策略
- 从盲目投机到理性投资:一位女股民的炒股心路历程
- 深度解析“龙空龙”中的“空”——空仓智慧与交易哲学
- 弱市中的智慧:精准仓位管理,守护投资资金
当前版本:V3.0

 VIP复盘网
VIP复盘网
