
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
信立泰
002294 |
-1.09%
|
最新:49.98
开盘:50.54 昨收:50.53 |
开盘%:0.02%
振幅%:2.57% 换手%:0.72% |
最高:51.19
最低:49.89 量比:0.85 |
总市值:557 亿
流通值:557 亿 成交额:11 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
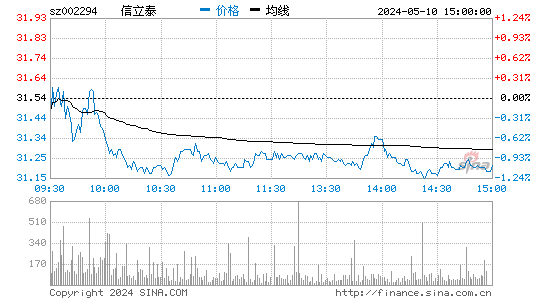
- 分时图
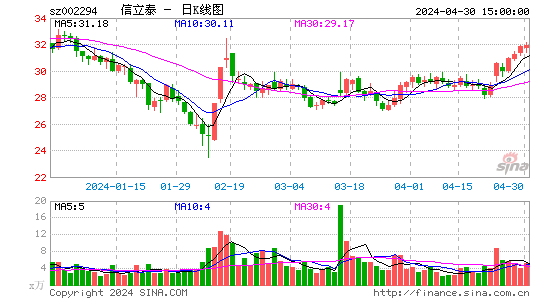
- 日K图
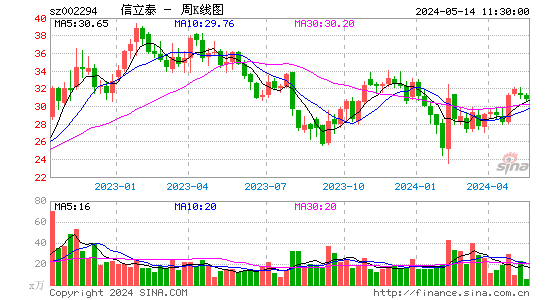
- 周K图
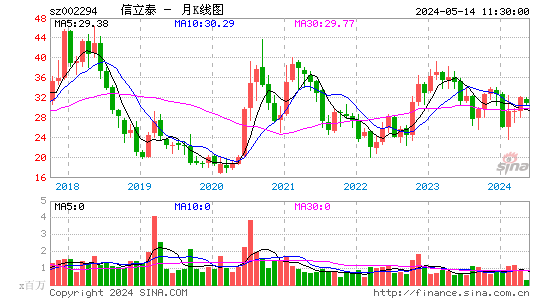
- 月K图
信立泰股票概况
全面了解信立泰股票及其公司背景
公司概况
信立泰药业股份有限公司是一家专注于心血管、抗肿瘤、降血糖等重大疾病领域的医药企业。公司自成立以来,凭借强大的研发实力和丰富的产品线,赢得了市场的广泛认可。
业务领域
信立泰在心血管领域有着深厚的技术积累,推出了一系列创新药物。同时,公司还积极拓展抗肿瘤、降血糖等其他重大疾病领域,形成了多元化的产品结构。
财务状况
近年来,信立泰的财务表现稳健。随着业务的不断拓展和市场份额的提升,公司的盈利能力持续增强。投资者对信立泰的未来发展充满信心。
未来发展
展望未来,信立泰将继续加大研发投入,推动更多创新药物的上市。同时,公司还将积极寻求外部合作,拓展国内外市场,实现业务的持续增长。
总结
信立泰作为医药行业的佼佼者,凭借强大的研发实力和多元化的产品结构,在市场中占据了一席之地。投资者对信立泰股票的前景持乐观态度。
2025-07-15 17:03
【尧唐生物YOLT-101获国家药监局临床试验批准,用于治疗家族性高胆固醇血症】7月14日,尧唐生物(YolTech Therapeutics)宣布,由尧唐生物与深圳信立泰药业股份有限公司联合申报的YOLT-101注射液临床试验申请已正式获得国家药品监督管理局药品审评中心(CDE)批准。YOLT-101拟开发适应症杂合子家族性高胆固醇血症(HeFH)。
2025-07-14 15:51
信立泰:YOLT-101获得临床试验默示许可。
2025-07-04 18:47
【重磅AI医疗政策出台,19股值得关注】7月4日电,根据北京市人民政府官网消息,为加快培育新质生产力,将北京打造成具有国际影响力的“人工智能+医药健康”创新高地,北京市科学技术委员会、中关村科技园区管理委员会、北京市卫生健康委员会等部门联合制定《北京市加快推动“人工智能+医药健康”创新发展行动计划(2025—2027年)》。证券时报·数据宝梳理了A股市场上部分AI医疗概念股,供读者参考。2025年以来,多只AI医疗概念股表现良好,贝瑞基因、安必平、信立泰涨幅居前,依次为73.37%、69.83%、55.34%;卫宁健康、艾隆科技、泓博医药、药明康德、迪安诊断等股涨幅均超过30%。
2025-06-17 23:01
【4股获北向资金龙虎榜净买入】6月17日电,今日龙虎榜现身个股中,4股获北向资金净买入,净买入居首的是赢合科技,金额为2826.91万元;信立泰、泰禾股份、超讯通信获净买入金额均超300万元。北向资金净卖出的有8股,恒宝股份遭净卖出1.04亿元,居首。
2025-06-17 10:46
创新药概念冲高回落,科兴制药跌超10%,百洋医药、华纳药厂跌超7%,信立泰、康弘药业、益方生物、迪哲医药等跟跌
2025-06-04 17:47
信立泰:阿利沙坦酯吲达帕胺缓释片(复立安)获得药品注册证书
2025-05-27 15:59
信立泰:沙库巴曲阿利沙坦钙片(信超妥)获得药品注册证书。
2025-05-27 15:58
【信立泰:沙库巴曲阿利沙坦钙片(信超妥)获得药品注册证书】5月27日电,信立泰(002294.SZ)公告称,公司收到国家药品监督管理局核准签发的沙库巴曲阿利沙坦钙片(信超妥)药品注册证书。该药品为公司独家研发的新药,本次获批的适应症为原发性高血压。信超妥是我国原研第一款、全球第二款获批的ARN I类药物,化合物专利保护期至2037年。Ⅲ期临床研究结果表明,其降压疗效显著并呈明显的剂量依赖性。信超妥的上市将对公司今后的业绩提升和长远发展产生积极的影响,但具体销售情况将受市场环境变化等因素的影响,存在一定的不确定性。
2025-05-23 13:42
创新药概念股持续走高,信立泰、科伦药业双双创历史新高,阳光诺和冲击20CM涨停,众生药业此前涨停,海辰药业、贝达药业、泓博医药涨超10%,舒泰神、海翔药业、泰格医药、华海药业等多股涨超5%。
2025-05-12 09:34
【创新药概念集体大跌 百济神州跌超8%】5月12日电,早盘创新药概念集体回调,迈威生物跌超10%,百济神州、信立泰双双跌超8%,益方生物、舒泰神、热景生物、百利天恒、诺诚健华等跌幅靠前。消息面上,特朗普将签署行政令,药价将立即降低30%-80%。
2025-05-07 10:42
创新药概念震荡回落,百济神州跌超7%,荣昌生物、益方生物、一品红、信立泰、迪哲医药等跌幅居前
2025-04-22 13:42
【医药板块持续走高 众生药业等多股涨停】4月22日电,午后医药板块持续走高,创新药方向继续领涨,众生药业、华森制药、富士莱涨停,百利天恒、诺诚健华、新诺威、百济神州创历史新高,复旦张江、上海谊众、信立泰、热景生物等涨幅靠前。消息面上,4月25日至4月30日,美国癌症研究协会(AACR)年会将在芝加哥召开。作为全球规模最大的癌症研究会议之一,AACR年会一直是癌症领域最新研究成果的重要展示平台。
2025-04-22 10:45
【创新药概念股反复活跃 百利天恒续创历史新高】4月22日电,百利天恒续创历史新高,华纳药厂涨超10%,东诚药业、上海谊众、众生药业、热景生物涨超5%,翰宇药业、信立泰、华森制药、新诺威等跟涨。消息面上,国元证券研报指出,在创新药领域,目前我国创新药研发逐步加速,部分领域已经达到世界前沿水平,对来自美国的进口药品增加关税,同样有助于国内同类创新药产品的进口取代。
2025-03-24 11:04
【深圳:政企医联动,共谋罕见病医药发展创新】3月20日上午,深圳市发展改革委(市药械办)联合市卫生健康委、市医保局,在河套深港科技创新合作区信立泰创新药发现中心召开“罕见病药院企座谈会”。会议汇聚政府、医院、企业三方力量,共谋罕见病诊疗生态建设,推动政策、临床与研发深度协同。接下来,深圳市将从资金支持、临床试验、用药支付等三个方面发力,努力克服罕见病药物研发多重挑战,持续推动罕见病药物在我市差异化布局和取得更多实效,致力打造全球罕见病防治标杆城市。(证券时报)
2025-02-13 17:31
信立泰:SAL0140药品临床试验申请获得受理
2025-01-20 15:48
信立泰:JK07在HFrEF(射血分数降低的心衰)和HFpEF(射血分数保留的心衰)患者的MRCT II期临床试验中获得积极的中期数据。
2025-01-20 15:44
【信立泰:JK07境外临床试验取得积极中期数据】1月20日电,信立泰公告,公司收到子公司Salubris Bio通知,JK07在HFrEF和HFpEF患者的MRCT II期临床试验中获得积极中期数据。JK07的II期临床研究中期分析旨在评估其在低剂量组(0.045mg/kg)的安全性,为启动高剂量组(0.09mg/kg)提供保障。根据中期分析结果,已启动高剂量组的患者入组。JK07的II期临床试验为随机、双盲、安慰剂对照、剂量递增研究,旨在评估其在HFrEF和HFpEF患者中的安全性和有效性。试验计划纳入282例心衰患者,本次中期分析纳入了最初随机的68名患者。数据显示,JK07在低剂量组中显示出良好的安全性和耐受性,两组在不良事件的发生频率和严重性方面无显著差异,并初步观察到积极疗效信号。JK07是公司自主研发、具有全球知识产权的NRG-1融合抗体药物,是心衰领域首个进入临床开发阶段的抗体融合蛋白、选择性ErbB4激动剂,拟开发适应症包括HFrEF和HFpEF。
2024-11-28 16:00
信立泰:阿利沙坦酯氨氯地平片(复立坦)、苯甲酸福格列汀片(信立汀)新纳入国家医保目录。
2024-11-16 18:34
【2023年度中国医药企业研发指数百强榜单发布,多家上市公司领跑】由工业和信息化部与上海市政府举办的中国医药工业发展大会日前召开。会上发布的2023年度中国医药企业研发指数显示,恒瑞医药、安图生物以及信达生物在医药创新赛道实力领跑。据了解,恒瑞医药凭借其研发实力和创新能力,综合排名第一。紧随其后的是安图生物、信达生物、春立医疗、信立泰、贝达药业、恩华药业、白云山、达安基因、迪哲医药、百济神州、九强生物、新华医疗、以岭药业、四环医药、复星医药、百奥泰、易瑞生物、启明医疗-B及石药集团等。(上证报)
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 精准捕捉个股卖点:K线图与移动平均线的智慧交融
- 短线操作的雷区:新手必知的八大禁忌
- 揭秘涨停股的“瞄准器”:异动K线与九阳真经
- 短线交易的艺术:洞悉市场,精准出击
- 潜伏以待,智取股市:中小散户的选股与潜伏策略
- 大盘与个股:投资策略的智慧抉择
- 揭秘股市奥秘:精准定位个股底部策略
- 主力试盘策略深度剖析:揭秘市场操控的艺术
- 洞察股市龙头奥秘,精准捕捉市场脉搏
- 精准捕捉优质成长股:选股策略与时机把握
- 全球视野下的A股“慢牛”格局解析
- 揭秘均线交易法则:五三买卖策略实战解析
- 股市盈利秘籍:揭秘四种典型交易者及其成功之道
- 透视股市庄家策略:揭秘下影线背后的市场转折信号
- 揭秘消费股内在价值:从吉列到中国消费品企业的成长之路
- 股市风云:深入剖析六种量价关系及其策略应用
- 揭秘股市神秘信号:精准捕捉揉搓线起涨点策略
- 从盲目投机到理性投资:一位女股民的炒股心路历程
- 深度解析“龙空龙”中的“空”——空仓智慧与交易哲学
- 弱市中的智慧:精准仓位管理,守护投资资金
当前版本:V3.0

 VIP复盘网
VIP复盘网
