
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
百利天恒
688506 |
6.7%
|
最新:321.04
开盘:297.78 昨收:300.88 |
开盘%:-1.03%
振幅%:10.63% 换手%:1.48% |
最高:324.49
最低:292.5 量比:1.56 |
总市值:1287 亿
流通值:330 亿 成交额:1 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
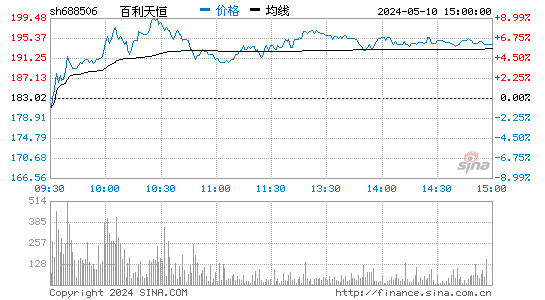
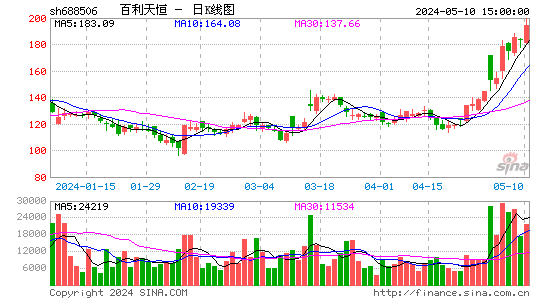
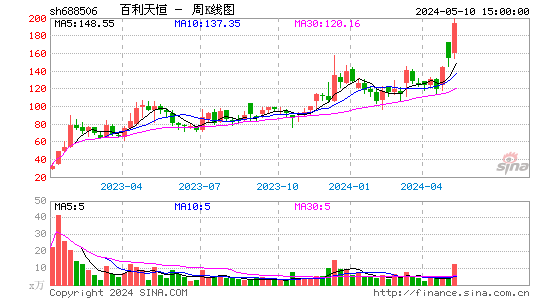
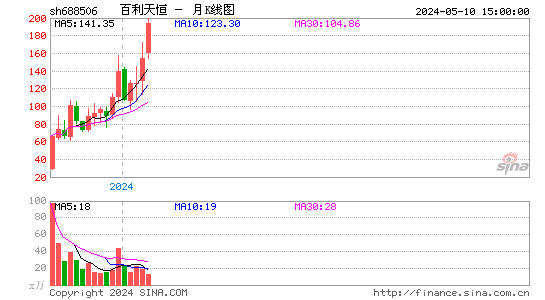
百利天恒-U股票详解
聚焦创新生物药的生物医药企业股票分析
公司概况
百利天恒-U,全称为四川百利天恒药业股份有限公司,成立于2006年8月17日,并于2023年1月6日上市。公司聚焦于全球生物医药前沿领域,致力于解决临床未被满足的需求。
业务与研发能力
百利天恒-U具备包括小分子化学药、大分子生物药及ADC药物的全系列药品研究开发能力。公司拥有从中间体、原料药到制剂的一体化优势,以及覆盖“研发—生产—营销”的完整全生命周期商业化运营能力。
业绩与市场表现
近年来,百利天恒-U的业绩表现亮眼。公司2024年营收预增932%,净利润约36亿元,实现了扭亏为盈。在股市方面,百利天恒-U的股价呈现波动上涨趋势,总市值和流通市值持续增长。
创新药物研发进展
百利天恒-U在创新药物研发方面取得了显著进展。公司自主研发的创新生物药注射用BL-M07D1(HER2-ADC)获得了III期临床试验的批准,这对于公司在乳腺癌治疗领域的布局具有重要意义。
未来展望
展望未来,百利天恒-U将继续聚焦创新生物药的研发,加速推进临床试验进程,争取早日将更多创新药物推向市场,以满足患者的临床需求。
总结:
百利天恒-U作为生物医药领域的佼佼者,凭借强大的研发能力和优异的市场表现,赢得了投资者的广泛关注。未来,随着创新药物的陆续上市,公司有望迎来更加广阔的发展前景。
2025-07-14 15:51
百利天恒:iza-bren(EGFR×HER3双抗ADC)联合用药治疗晚期肾癌获得II期药物临床试验批准通知书。
2025-07-02 17:41
【百利天恒:iza-bren在治疗鼻咽癌的III期临床试验中期中分析达到主要终点】2日讯,百利天恒(688506.SH)公告称,公司自主研发的全球首创EGFR×HER3双抗ADC药物iza-bren在鼻咽癌的III期临床试验中期中分析达到主要终点,适应症为既往经PD-1/PD-L1单抗治疗且经至少两线化疗(至少一线含铂)治疗失败的复发性或转移性鼻咽癌。该药物目前在中国和美国进行40余项针对多种肿瘤类型的临床试验,已有5项适应症被纳入突破性治疗品种名单。但需注意,药品从临床试验到投产周期长,存在不确定性因素影响。
2025-06-23 17:35
百利天恒:注射用BL-M07D1(HER2 ADC)用于在新辅助治疗后存在浸润癌残留的HER2阳性乳腺癌术后辅助治疗III期临床试验完成首例受试者入组
2025-06-16 07:31
【A股公司赴港上市提速 优质标的获国际长线资金抢筹】6月16日电,今年以来,A股行业龙头企业接连筹备赴港上市,拟构建“A+H”双融资平台。从进展来看,赛力斯、晶澳科技等公司已向中国证监会提交上市备案材料,百利天恒、奥克斯电气等公司已向香港交易所递交上市申请。安永大中华区上市服务主管合伙人何兆烽表示,拟“A+H”两地上市的企业多为细分领域龙头,具备较强稀缺性,可以吸引国际资本持续流入,使市场形成良性循环。未来,预计将有更多大型企业及产业链领军企业登陆港股。国际长线资金愈发热衷于参与优质港股IPO项目。“今年港股IPO的基石投资者认购踊跃。甚至在部分优质项目中,很多机构投资者拿不到基石认购额度,只能通过锚定方式参与。”高盛亚洲(除日本外)股票资本市场主管王亚军表示。(证券日报)
2025-06-07 18:08
【近一周280多只个股获机构调研 中微公司调研机构数最多】6月7日电,近一周机构调研个股数量有280多只,中微公司调研机构数最多。中微公司有212家机构调研,其中包括34家基金公司、61家证券公司、37家私募、7家保险公司等。华测检测、百利天恒、鼎泰高科、中科创达、海南华铁等个股近一周也有逾百家机构调研。其中,百利天恒作为创新药龙头股之一,市值超1200亿元,本周股价创出历史新高,最新收盘价在300元以上,是A股第九高价股。
2025-05-30 20:58
百利天恒:注射用BL-M07D1(HER2 ADC)用于HER2低表达复发或转移性乳腺癌III期临床试验完成首例受试者入组
2025-05-14 05:07
【明晟公司MSCI新增30只股票到MSCI ACWI指数 并从中剔除61只股票】5月14日电,明晟公司(MSCI)公布了5月份指数审议结果。MSCI全球股票指数(ACWI)新纳入30只股票,剔除61只股票。其中MSCI中国指数新纳入芯原股份、百利天恒、惠泰医疗、光线传媒、海思科等6只股票;剔除海信家电、一汽解放、上海医药、金诚信等17只股票。此次调整将于5月30日收盘后生效。由于MSCI中国指数被嵌套进MSCI新兴市场指数,因此股票进入MSCI中国指数,便意味着进入了MSCI全球标准指数系列,从而获得被动资金跟踪。
2025-05-12 09:35
创新药板块盘初下挫,迈威生物跌超10%,益方生物、舒泰神跌超9%,百济神州跌超8%,荣昌生物、百利天恒纷纷下挫
2025-05-12 09:34
【创新药概念集体大跌 百济神州跌超8%】5月12日电,早盘创新药概念集体回调,迈威生物跌超10%,百济神州、信立泰双双跌超8%,益方生物、舒泰神、热景生物、百利天恒、诺诚健华等跌幅靠前。消息面上,特朗普将签署行政令,药价将立即降低30%-80%。
2025-04-29 17:54
【百利天恒:一季度净亏损5.31亿元】4月29日电,百利天恒(688506.SH)公告称,公司2025年一季度营业收入为6744万元,同比下降98.77%,主要系上年同期确认了大额知识产权授权收入。一季度净亏损5.31亿元,去年同期净利润50.05亿元,主要系营业收入减少和研发费用增加。
2025-04-28 11:03
创新药概念探底回升,博瑞医药涨超10%,股价创出4年多新高,诺思兰德、艾迪药业、百利天恒、荣昌生物、君实生物等涨幅靠前。
2025-04-22 16:25
百利天恒:BL-M11D1(CD33-ADC)联合用药治疗新诊断的急性髓系白血病获得药物临床试验批准通知书
2025-04-22 13:42
【医药板块持续走高 众生药业等多股涨停】4月22日电,午后医药板块持续走高,创新药方向继续领涨,众生药业、华森制药、富士莱涨停,百利天恒、诺诚健华、新诺威、百济神州创历史新高,复旦张江、上海谊众、信立泰、热景生物等涨幅靠前。消息面上,4月25日至4月30日,美国癌症研究协会(AACR)年会将在芝加哥召开。作为全球规模最大的癌症研究会议之一,AACR年会一直是癌症领域最新研究成果的重要展示平台。
2025-04-22 10:45
【创新药概念股反复活跃 百利天恒续创历史新高】4月22日电,百利天恒续创历史新高,华纳药厂涨超10%,东诚药业、上海谊众、众生药业、热景生物涨超5%,翰宇药业、信立泰、华森制药、新诺威等跟涨。消息面上,国元证券研报指出,在创新药领域,目前我国创新药研发逐步加速,部分领域已经达到世界前沿水平,对来自美国的进口药品增加关税,同样有助于国内同类创新药产品的进口取代。
2025-04-15 17:25
百利天恒:BL-B01D1(EGFR×HER3双抗ADC)联合用药治疗多种晚期实体瘤获得4个II期药物临床试验批准通知书
2025-04-08 15:47
百利天恒:BL-B01D1(EGFR×HER3双抗ADC)用于在局部晚期或转移性尿路上皮癌III期临床试验完成首例受试者入组。
2025-04-07 13:14
【生物医药股集体大跌 相关公司回应关税影响】4月7日电,美国挥下关税“大棒”后,4月7日,亚太股市恐慌情绪蔓延,生物医药股大跌。“股价暴跌反映了投资人的恐慌,资本市场可能认为美国的关税政策对医药行业仍然有影响,尽管在我们看来,这种担心被放大了。”一位上市公司创新药相关业务负责人对记者表示。一位美国医药投资人也对记者表示:“中国生物药企股价暴跌更像是一种情绪的宣泄,几乎所有的公司都在跌,但实际上我们认为关税对创新药的影响目前还看不出来。”百利天恒董事长朱义4月6日回应“对等关税”对我国生物医药企业出海的影响时称,截至目前,“对等关税”针对的是商品贸易方向,尚未针对创新药授权交易等知识产权方向。他认为,我国生物医药行业对美商品贸易以仿制药出口为主,国产创新药的出口额相对较少,许可授权的交易额更大,但这些交易暂不受关税冲击;而对于在美有较强市场潜力的国产创新药,未来若要出口,受益于国内生产的低成本和美国市场的高售价也完全具备承受能力。另一位不愿透露姓名的国内创新药企业高管对记者表示:“医药行业在贸易关税政策中的地位比较特殊。目前我们公司生产的生物制剂产品是美国国内稀缺的,美国预计不会针对国内稀缺品进行重点打击。” (第一财经)
2025-03-28 19:52
【百利天恒:2024年净利润37.08亿元 同比扭亏为盈】28日讯,百利天恒(688506.SH)发布2024年年度报告,报告期内公司实现归属于上市公司股东的净利润37.08亿元,较上年同期增加44.88亿元,实现扭亏为盈。公司2024年度利润分配预案为:不派发现金红利,不送股,不以资本公积金转增股本。
2025-03-27 15:41
【今日投资舆情热点】1)化工:近期,包括双季戊四醇、溴素、硫酸等多个化工品价格均快速上涨。2)半导体芯片:新凯来通过照片和模型的方式展示了其多款即将发布的产品,已开发6大类半导体工艺和量检测装备。3)创新药:2024年,大约31%的大型跨国药企引进的创新药候选分子来自中国,百利天恒、和誉医药等多家企业2024年转亏为盈,授权交易带来的收入发挥了关键作用。4)金融:央行副行长宣昌能表示,中国明确适度宽松的货币政策,将根据国内外经济金融形势择机降准降息。
2025-03-27 13:09
创新药板块持续走高,迈威生物午后涨超10%,百利天恒、泽璟制药、康弘药业、诺诚健华、益方生物、热景生物等多股涨超7%
2025-03-12 10:43
【百利天恒在成都新设生物科技公司】企查查APP显示,近日,成都诺芯生物科技有限公司成立,法定代表人为朱义,注册资本300万元,经营范围包含:技术服务、技术开发、技术咨询、技术交流、技术转让、技术推广;技术进出口;货物进出口。企查查股权穿透显示,该公司由百利天恒全资持股。
2025-03-09 15:45
【百利天恒:拟定增募资不超39亿元,用于创新药研发项目】百利天恒公告,公司拟向特定对象发行股票募资不超过39亿元,扣除发行费用后将全部用于创新药研发项目。
2025-03-02 16:26
【百利天恒:创新生物药Ⅲ期临床试验完成首例受试者入组】百利天恒公告,公司自主研发的创新生物药注射用BL-B01D1(EGFR×HER3双抗ADC)联合奥希替尼用于一线EGFR突变型局部晚期或转移性非小细胞肺癌Ⅲ期临床试验完成首例受试者入组。截至目前,BL-B01D1正在中国和美国进行约30项针对多种肿瘤类型的临床试验,除此次新入组的临床试验外,BL-B01D1在肺癌、乳腺癌、鼻咽癌、食管鳞癌等7项国内III期注册临床试验也处于受试者入组的阶段。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 如何慧眼识珠,捕捉大牛股:深入解析成长股选择策略
- 可转债交易的盈利之道:坚守与认知的力量
- 周期股估值的脉动:揭秘波动规律与价值挖掘
- 成为市场高手的全方位准则与深度剖析
- 冬季投资藏宝图:洞悉股市季节性热点与策略
- 解锁主升浪密码:深度剖析高度、晋级率与容错率
- 融资融券操作指南:精通融资买入与融券卖出策略
- 跟大师脚步,掌握马尔基尔投资五原则,稳健前行
- 熊市抄底:坚守底线,智慧投资
- 可转债价值评估全解析:掌握关键指标,精准捕捉投资机会
- 超短线操作的艺术:揭秘高手策略与实战智慧
- 掌握KDJ指标,解锁股市短线交易密钥
- 连板梯队解析与短线策略精髓
- 炒股稳赚之道:三步策略与自我超越
- 揭秘盘感之源:塑造卓越操盘能力的多维度探索
- 深入解析炒股常用均线的实盘作用
- 揭秘股市波动:如何精准捕捉主力建仓信号
- 掌握卖出股票的艺术:策略与心理解析
- 股市成交量定律深度剖析与实战应用
- 掌握日内短线交易的高级技巧
当前版本:V3.0

 VIP复盘网
VIP复盘网
