
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
亚虹医药
688176 |
1.96%
|
最新:12.46
开盘:12.25 昨收:12.22 |
开盘%:0.25%
振幅%:3.52% 换手%:4.36% |
最高:12.6
最低:12.17 量比:2.02 |
总市值:71 亿
流通值:54 亿 成交额:4 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
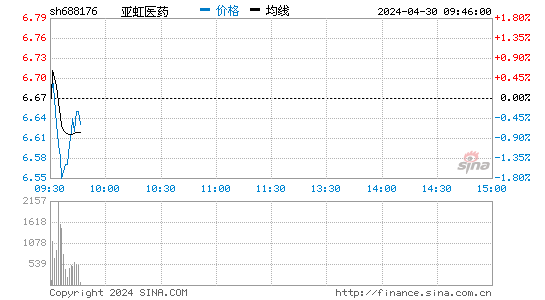
- 分时图
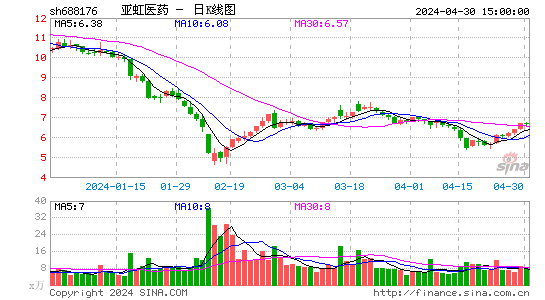
- 日K图
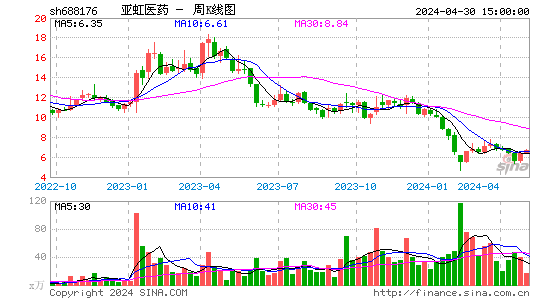
- 周K图
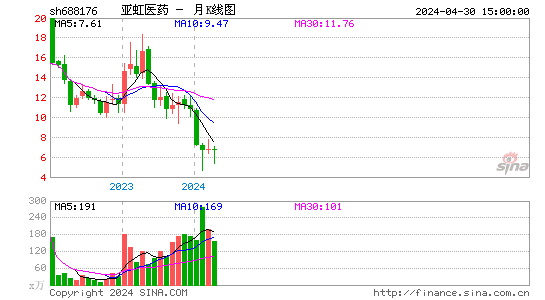
- 月K图
亚虹医药-U股票概览
从基本信息到市场表现全面解析
一、基本信息
亚虹医药-U是一家专注于生物医药领域的上市公司,致力于新药研发和市场推广。其股票在科创板上市,吸引了众多投资者的目光。
二、市场表现
股票行情:亚虹医药-U的股票价格近期呈现波动。截至最新交易日,其股价及成交量等数据可根据实时市场行情获取。
融资情况:公司近期多次获得融资买入,显示出市场对其未来发展的认可。例如,2025年2月6日,亚虹医药获融资买入258.54万元。
三、业绩与前景
业绩预告:亚虹医药预计2024年年报净利润将出现亏损,预计在-4.37亿元到-3.66亿元之间。
产品研发:公司在膀胱癌检查和治疗领域有显著成果,其显影剂产品APL-1706已获得国家药品监督管理局核准签发的《药品注册证书》。
四、核心技术人员调整
2025年初,亚虹医药宣布调整核心技术人员。此次调整可能对公司研发实力和创新能力产生影响,值得投资者密切关注。
总结
亚虹医药-U作为生物医药领域的上市公司,其市场表现、业绩与前景以及核心技术人员调整等信息均对投资者具有重要意义。尽管面临业绩亏损等挑战,但公司在产品研发和市场拓展方面仍有潜力可挖。
2025-07-14 10:06
医药股反复活跃,沃华医药拉升封板,联环药业、康辰药业、诚意药业此前涨停,亚虹医药、莱美药业涨超10%。
2025-06-19 17:32
【32家科创板未盈利公司将纳入科创成长层】6月19日电,6月18日,中国证监会发布《关于在科创板设置科创成长层增强制度包容性适应性的意见》,明确设置科创板科创成长层。上海证券交易所起草了《上海证券交易所科创板上市公司自律监管指引第5号——科创成长层(征求意见稿)》(下称《科创成长层指引》),从科创成长层的层次定位、纳入调出条件、信息披露要求、风险揭示等方面作出具体要求。据记者统计,科创板累计已有54家未盈利企业上市。目前已有22家企业上市后实现盈利,还有32家尚未实现摘“U”。根据《科创成长层指引》要求,上述32家公司将自指引(正式稿)发布之日起纳入科创成长层。具体来看,32家尚未摘“U”的存量公司包括:泽璟制药、君实生物、前沿生物、青云科技、和辉光电、精进电动、百济神州、迪哲医药、迈威生物、翱捷科技、亚虹医药、首药控股、海创药业、云从科技、益方生物、奥比中光、盟科药业、诺诚健华、信科移动、星环科技、裕太微、云天励飞、天智航、奇安信、寒武纪、亿华通、埃夫特、慧智微、芯联集成、智翔金泰、盛科通信、中巨芯。(上海证券报)
2025-03-13 17:29
亚虹医药:APL-2302完成Ⅰa期临床首例受试者入组。
2025-02-14 17:03
亚虹医药:APL-1202口服联合替雷利珠单抗新辅助治疗肌层浸润性膀胱癌试验在2025年美国临床肿瘤学会泌尿生殖系统肿瘤研讨会上发布Ⅱ期临床试验数据
2024-11-12 17:00
【亚虹医药:APL-1702临床试验结果入选2024年IPVC】亚虹医药公告,近日,公司产品APL-1702用于治疗宫颈高级别鳞状上皮内病变的前瞻、随机、双盲、安慰剂对照的国际多中心Ⅲ期临床试验结果入选2024年国际乳头瘤病毒大会(IPVC),并以壁报形式发布本研究关于不同HPV型别、不同随访时间的HPV清除率分析数据。目前上述产品的上市申请已获国家药监局受理,尚需经过审评、药品临床试验现场检查、药品生产现场检查和审批等环节,上述产品能否成功上市及上市时间具有不确定性。
2024-11-05 17:32
【亚虹医药:灌注用盐酸氨酮戊酸己酯获批上市】亚虹医药公告,公司收到国家药监局核准签发的《药品注册证书》,批准公司APL-1706(灌注用盐酸氨酮戊酸己酯)上市。灌注用盐酸氨酮戊酸己酯用于膀胱癌(包括原位癌)患者的膀胱镜检查等。
2024-10-24 17:23
【亚虹医药:APL-2302临床试验申请获得FDA批准】亚虹医药公告,近日公司收到美国食品药品监督管理局(简称“FDA”)关于同意开展公司自主研发的APL-2302用于治疗晚期实体瘤临床试验的函告。APL-2302临床试验申请获FDA批准后,公司将尽快向中国国家药品监督管理局(NMPA)药品审评中心(CDE)递交新药临床试验申请(IND),积极推动该项临床试验在全球范围内的开展。本次APL-2302临床试验申请获得FDA批准事项对公司近期业绩不会产生重大影响。
2024-09-17 15:50
【亚虹医药:APL1702用于治疗HSIL的国际多中心Ⅲ期临床试验结果入选2024年国际光动力与光诊断大会】亚虹医药9月17日晚间公告,近日,公司产品APL1702用于治疗宫颈高级别鳞状上皮内病变(HSIL)的前瞻、随机、双盲、安慰剂对照的国际多中心Ⅲ期临床试验结果入选2024年国际光动力与光诊断大会,并以大会口头报告的形式发布该研究关于降低宫颈癌前病变组织病理学分级的疗效数据。来自中国、德国、荷兰等多个国家的402名符合条件的患者随机化后入组该研究。已完成的统计分析结果显示,该研究已达到主要疗效终点,安全性良好。
2024-06-24 18:52
【亚虹医药:APL-1202临床试验申请获批】亚虹医药公告,公司收到国家药监局签发的《药物临床试验批准通知书》,公司APL-1202用于治疗自由生活阿米巴(Free-living Amoebae,FLA)感染的临床试验申请获得批准。
2024-05-12 21:49
【亚虹医药:盐酸氨酮戊酸己酯软膏光动力治疗系统上市申请获得受理】亚虹医药公告,收到国家药品监督管理局核准签发的《受理通知书》,公司产品APL-1702(通用名:盐酸氨酮戊酸己酯软膏光动力治疗系统)拟用于治疗18岁及以上排除原位癌的经组织学证实的宫颈高级别鳞状上皮内病变(High-Grade Squamous Intraepithelial Lesion, HSIL)患者的上市申请获得受理。
2024-05-12 16:00
【亚虹医药:盐酸氨酮戊酸己酯软膏光动力治疗系统上市申请获得受理】5月12日电,亚虹医药公告,收到国家药品监督管理局核准签发的《受理通知书》,公司产品APL-1702(通用名:盐酸氨酮戊酸己酯软膏光动力治疗系统)拟用于治疗18岁及以上排除原位癌的经组织学证实的宫颈高级别鳞状上皮内病变(High-Grade Squamous Intraepithelial Lesion, HSIL)患者的上市申请获得受理。
2024-04-23 13:33
【创新药概念股震荡拉升 首药控股等多股涨超5%】4月23日电,首药控股、迪哲医药、荣昌生物、凯因科技、吉贝尔、百利天恒、亚虹医药等多股涨超5%。消息面上,近日北京市医疗保障局、北京市药品监督管理局等多部门发布北京市支持创新医药高质量发展若干措施(2024)。
2024-03-19 09:34
【AI医疗概念延续强势 塞力医疗2连板】3月19日电,AI医疗概念延续昨日强势,塞力医疗、贝瑞基因2连板,阿拉丁、泓博医药涨超7%,亚虹医药、安必平等跟涨。消息面上,英伟达此次GTC大会上在医疗场景上推出了基于医疗场景的25个新的微服务(NIM), 帮助全球的医疗保健公司可以基于生成式 AI进行效率提升。
2024-03-18 15:41
【亚虹医药:发布APL-1702用于治疗宫颈高级别鳞状上皮内病变的国际多中心Ⅲ期临床试验数据】18日讯,亚虹医药公告,近日公司产品APL-1702用于治疗宫颈高级别鳞状上皮内病变的前瞻、随机、双盲、安慰剂对照的国际多中心Ⅲ期临床试验结果入选2024年欧洲生殖器官感染和肿瘤研究组织大会(EUROGIN)和2024年美国妇科肿瘤学会年会(SGO),并均以大会口头报告的形式发布本研究关于疗效和安全性的核心数据。
2024-03-18 15:40
亚虹医药:在2024年EUROGIN和SGO会议上发布APL-1702用于治疗宫颈高级别鳞状上皮内病变的国际多中心Ⅲ期临床试验数据。
2024-03-02 10:54
【1016家公司公布业绩快报:50%去年净利润增长】统计显示,公布业绩快报的1016家公司中,营业收入最高的是保利发展,去年实现营业收入3471.47亿元,同比增长23.49%;其次是宝钢股份、招商银行,去年营业收入分别为3469.26亿元、3391.23亿元。增幅方面,639家公司营业收入同比增长,增幅最高的是亚虹医药,去年实现营业收入0.14亿元,同比增长52594.64%;其次是迈威生物、中自科技,营业收入同比分别增长360.49%、245.14%。(第一财经)
2024-02-06 19:16
亚虹医药:拟以5000万元-1亿元回购股份,回购股份的价格不超过人民币12.80元/股
2024-02-04 20:34
【近20家上市公司今日披露回购或增持计划公告 杉杉股份拟最高5亿元回购股份 绝味食品和立昂微回购用于注销】2月4日电,截至发稿,据不完全统计,今日包括杉杉股份、绝味食品、水井坊、立昂微、逸飞激光、联创光电、中泰股份、长阳科技、涛涛车业、恒锋工具、亚虹医药、五洋停车、普源精电、奥比中光、南微医学、京源环保、同方股份、红豆股份和科力远在内的19家A股上市公司披露回购或增持计划公告。具体来看,16家公司披露回购计划公告。其中杉杉股份拟以2.5亿元-5亿元回购股份,涉及金额最大;绝味食品和立昂微均表示回购公司股份拟用于注销等。此外,三一重能公告董事长提议将回购股份金额提高至3亿元-5亿元。4家上市公司披露增持计划公告。其中同方股份间接控股股东及其一致行动人拟不超5亿元增持公司股份。
2024-02-04 17:50
【亚虹医药:APL-1202数据发布,未来将继续深耕膀胱癌领域拓展更多可能】亚虹医药公布APL-1202与化疗灌注联合使用二线治疗化疗灌注复发的中高危非肌层浸润性膀胱癌(NMIBC)的关键性临床试验数据显示公告,在部分患者人群中显示出一定的优效趋势,但试验未达到主要研究终点。除上述临床外,亚虹医药同时正在开展APL-1202其他临床试验。此前公司公布的APL-1202口服联合PD-1免疫抑制剂替雷利珠单抗作为肌层浸润性膀胱癌(MIBC)新辅助治疗的Ⅱ期临床试验已完成期中分析数据,并取得了积极结果。
2023-12-24 16:27
【亚虹医药:APL-2301在澳大利亚开展Ⅰ期临床试验获许可】亚虹医药公告,公司子公司MetCuraPharmaceuticals AUS Pty Ltd收到澳大利亚人类研究伦理委员会签发的关于批准公司开发的用于治疗鲍曼不动杆菌感染的产品APL-2301(此为更新后编号,原编号为ASN-1733)开展Ⅰ期临床试验的临床试验伦理许可。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 股市逆势盈利策略:精准捕捉机遇,稳健驾驭风险
- 运用MACD研判趋势拐点:交叉、背离与综合应用
- 股市投资准则:稳健决策,智取胜利
- 短线高手的实战宝典:精准看盘与策略布局
- ASI+CCI指标组合:解锁股票震荡趋势的买卖密码
- 捕捉龙头,制胜股市 —— 深度解析个股上涨初期板块龙头判断法
- 揭秘股市迷雾:个股盘口特殊现象深度剖析
- 游资与主力拉升股价的差异化解析
- 十字星研判秘籍:解锁行情走向的四大钥匙
- 识破市场迷雾,洞悉真假上涨之道
- 把握市场脉搏,提升一进二策略成功率
- 股市迷思:揭秘赔钱思维,探寻盈利之道
- 掌握四大绝技,精准预判大盘走势
- 低吸的艺术:掌握震荡节奏,精准捕捉市场机遇
- 股市智慧:精准捕捉低位吸筹的黄金时机
- 短线高手的必备秘籍:精准控制回撤的策略与实践
- 投资大师的智慧:面对股市跌市的三大黄金策略
- 如何看大盘:走出涨跌焦虑症,提升战略定力
- 通过四根K线洞察股市大盘底部信号
- 炒股高手的逃顶秘籍:八大招助你规避风险
当前版本:V3.0

 VIP复盘网
VIP复盘网
