JAK抑制剂:靶向JAK-STAT通路的AD治疗药物
时间:2026-05-07 13:38
上述文章报告出品方/作者:阳光诺和;仅供参考,投资者应独立决策并承担投资风险。
特应性皮炎是一种慢性、复发性、炎症性皮肤病,以剧烈瘙痒、皮肤干燥和湿疹样皮损为特征。近二十年来,研究明确了Th2型免疫反应(包括IL-4、IL-13、IL-31等)在发病中的核心作用。2017年,靶向IL-4Rα的单抗度普利尤单抗获批,开启精准医疗时代。同时,多种关键细胞因子均通过JAK-STAT通路传导信号。JAK抑制剂作为小分子药物,能同时阻断多条炎性信号,发挥广谱抗炎和抗瘙痒作用,成为治疗领域的重大突破。JAK抑制剂的作用机制
JAK的生物学功能
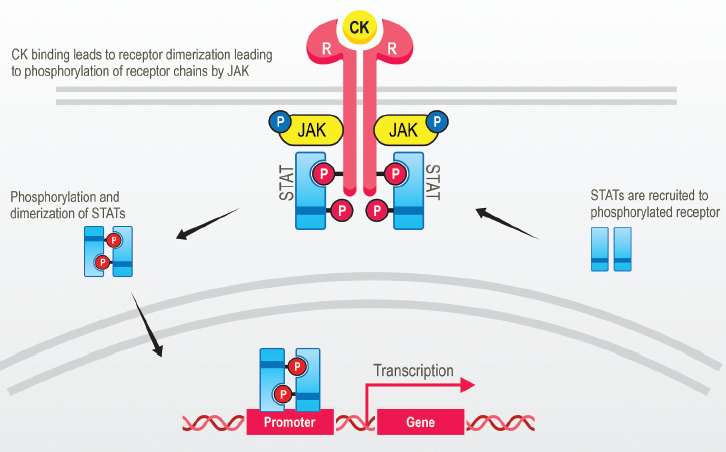
JAK是一类非受体型酪氨酸激酶,其名称源于罗马神话中的“两面神”Janus,因其结构域包含两个相似的磷酸转移结构域。JAK-STAT信号通路是细胞因子、生长因子等多种胞外信号向细胞核内传递的核心通路之一。当细胞因子与其相应受体结合后,导致受体构象改变,使得与之偶联的JAK激酶相互靠近并发生磷酸化而激活。活化的JAK继而磷酸化受体胞内段上的酪氨酸残基,为STAT蛋白提供结合位点。STAT蛋白通过其SH2结构域与受体上的磷酸化酪氨酸结合后,被JAK磷酸化。随后,磷酸化的STAT形成同源或异源二聚体,并转位进入细胞核内,与特定的DNA序列结合,从而调控靶基因的转录。该通路在细胞增殖、分化、凋亡、造血及免疫调节等众多生理过程中发挥关键作用。JAK的亚型
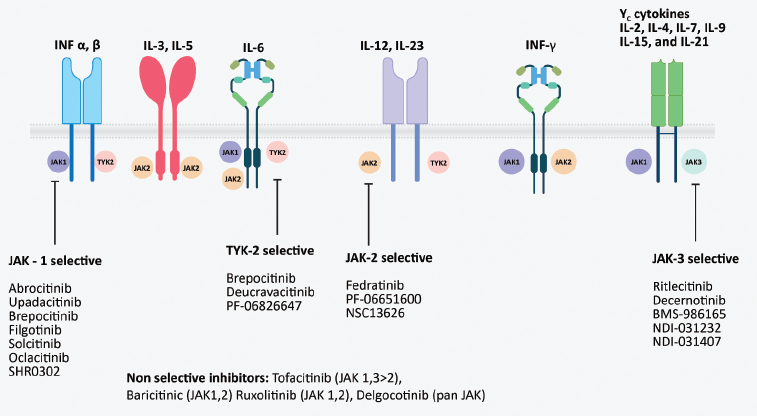
哺乳动物JAK家族包含四个成员:JAK1、JAK2、JAK3和TYK2,它们与不同细胞因子受体的胞内结构域特异性结合。其中,JAK1和JAK3主要介导γc细胞因子(如IL-2、IL-4、IL-7、IL-9、IL-15、IL-21)的信号;JAK1和TYK2介导I型干扰素及IL-10家族细胞因子的信号;JAK2主要与造血相关细胞因子(如促红细胞生成素、血小板生成素、GM-CSF)的受体偶联,也参与其他多种细胞因子信号传导。在特应性皮炎病理过程中,多种细胞因子依赖不同的JAK组合传递信号:IL-4、IL-13信号依赖于JAK1/JAK3和JAK1/TYK2,IL-31依赖于JAK1/JAK2,IL-22依赖于JAK1/TYK2,IFN-γ依赖于JAK1/JAK2。因此,JAK构成了连接多种炎性细胞因子的信号枢纽。JAK抑制剂的作用机制
JAK抑制剂是一类小分子药物,通过与JAK激酶结构域的ATP结合位点竞争性结合,抑制其磷酸化活性,从而阻断下游STAT激活及基因转录。不同抑制剂对四种JAK亚型的亲和力各异,因此选择性不同。第一代JAK抑制剂(如托法替布、芦可替尼、巴瑞替尼)抑制谱较宽,同时抑制多个JAK成员。虽疗效显著,但非选择性抑制JAK2可能导致贫血、血小板减少等血液学不良反应,广泛免疫抑制也增加感染风险。第二代JAK抑制剂(如乌帕替尼、阿布昔替尼、利特昔替尼)通过结构优化实现对特定亚型(如JAK1)的高选择性,在保留抗炎疗效的同时减少与JAK2、JAK3抑制相关的不良反应。在特应性皮炎中,选择性抑制JAK1可阻断IL-4、IL-13、IL-31、IL-22、TSLP等关键促炎和致痒细胞因子的信号,同时保留JAK2介导的造血功能,为选择性JAK1抑制剂的应用提供了理论基础。已上市的JAK抑制剂
目前已有多种JAK抑制剂在全球范围内获批用于治疗特应性皮炎,涵盖外用和口服两大剂型。外用制剂
外用JAK抑制剂为轻中度特应性皮炎患者提供了非激素类的新选择,其优势在于靶向作用于皮损局部,系统性吸收少,从而降低了全身性不良反应的风险。芦可替尼
芦可替尼1.5%乳膏是首个获FDA批准用于特应性皮炎的局部外用JAK1/2抑制剂。关键III期试验(TRuE-AD1/2)显示,治疗8周后,芦可替尼组达到IGA治疗成功的患者比例为53.8%和51.3%,显著优于安慰剂组(15.1%和7.6%)。患者用药2天内瘙痒显著缓解。儿童III期TRuE-AD3研究中,56.5%的2-11岁患儿达到IGA成功(安慰剂10.8%),疗效可持续1年。最常见不良反应为鼻咽炎、腹泻、支气管炎等,未观察到皮肤萎缩。德戈替尼
德戈替尼软膏是首创的泛JAK抑制剂,可同时抑制JAK1/2/3和TYK2。2020年在日本首次获批,后扩展至6个月以上儿童。日本III期试验显示,成人使用0.5%德戈替尼每日两次治疗4周后,mEASI改善率较安慰剂显著提高(-44.29% vs 1.74%);2-16岁儿童使用0.25%制剂亦显示优效。6个月至2岁婴幼儿治疗52周后mEASI改善率达-81.86%。局部暴露极低,最常见不良反应为应用部位毛囊炎、痤疮和刺激感,未观察到皮肤萎缩。托法替布
托法替布是第一代泛JAK抑制剂(主要抑制JAK1/3)。2%软膏被印度CDSCO获批用于轻中度特应性皮炎。II期研究中,治疗4周后EASI评分较基线改善81.7%,显著优于赋形剂组(29.9%),患者第2天瘙痒改善。III期试验显示疗效与吡美莫司1%软膏相当,EASI 50/75/90及瘙痒评分均显著改善。局部外用全身吸收极低,76%的血浆浓度<1.0 ng/mL,安全性窗口较口服制剂宽超12倍。不良事件发生率与吡美莫司组相当,无严重不良事件,未观察到口服JAK抑制剂相关的黑框警告风险。口服制剂
口服JAK抑制剂为那些对局部治疗应答不佳或不适合使用生物制剂的中重度特应性皮炎患者提供了高效、便捷的系统性治疗手段。乌帕替尼
乌帕替尼是高选择性JAK1抑制剂,已在中国、美国、欧洲等地区获批用于12岁及以上中重度特应性皮炎。III期研究(Measure Up 1/2、AD Up)显示,15mg或30mg每日一次治疗16周后,皮损清除(EASI-75、IGA 0/1)和瘙痒缓解均显著优于安慰剂,疗效维持52周。头对头Heads Up研究中,30mg组16周EASI-75应答率(71%)优于度普利尤单抗(61%),起效更快,第一周即显瘙痒优势。最常见不良事件为痤疮、上呼吸道感染、鼻咽炎和肌酸磷酸激酶升高。阿布昔替尼
阿布昔替尼是高选择性JAK1抑制剂,已在中国、美国和欧洲获批用于12岁及以上中重度特应性皮炎。III期JADE MONO-1/2证实,单药治疗12周后IGA 0/1和EASI-75应答显著优于安慰剂;MONO-1研究中200mg组EASI-75应答率62.7%,安慰剂组仅11.8%。头对头JADE COMPARE研究中,200mg组2周时瘙痒缓解率优于度普利尤单抗,展现快速止痒优势。最常见不良事件为恶心(剂量依赖性且自限性)、头痛、鼻咽炎和痤疮。巴瑞替尼
巴瑞替尼是JAK1/JAK2抑制剂,在欧洲、日本等地区获批用于成人中重度特应性皮炎。多项III期研究(BREEZE-AD1至AD7)证实,2mg或4mg每日一次联合外用糖皮质激素治疗,在改善皮损和瘙痒方面优于安慰剂。其疗效相对强效JAK1抑制剂(乌帕替尼、阿布昔替尼)稍显温和,但仍为患者提供有效治疗选择。安全性特征与其他JAK抑制剂相似,包括上呼吸道感染、鼻咽炎和带状疱疹风险增加。由于对JAK2的抑制,需关注潜在的血液学不良反应。在研的JAK抑制剂
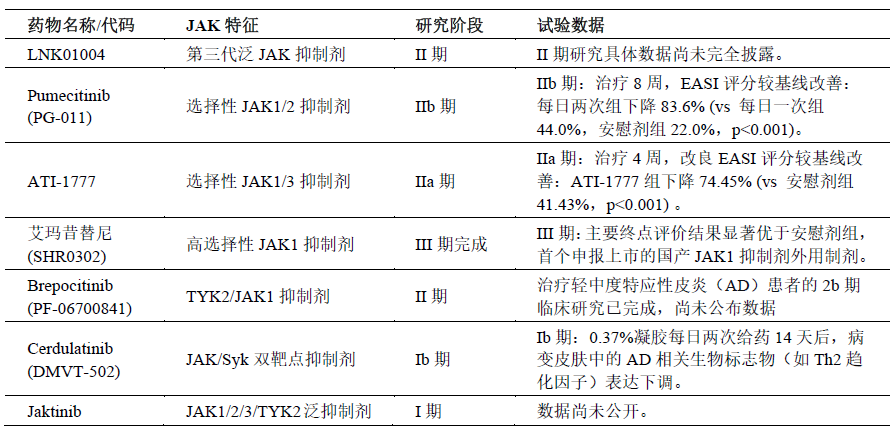
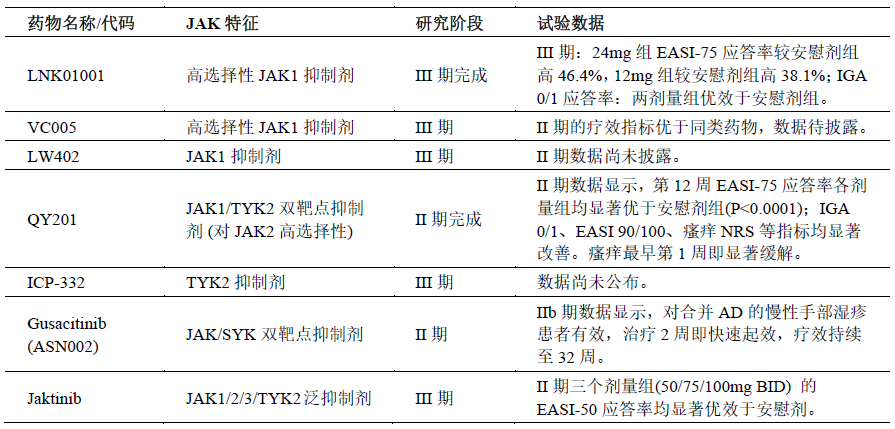
JAK抑制剂的研发管线依然活跃,多个新型药物正在进行临床研究,旨在进一步提高疗效、改善安全性或提供新的给药途径。结语
JAK抑制剂是特应性皮炎治疗的里程碑式突破。它们精准靶向多种炎性细胞因子汇聚的信号通路,起效迅速,尤其在缓解剧烈瘙痒方面优势显著,且口服给药比生物制剂更便利。当前临床已拥有多元选择:高效口服JAK1抑制剂(乌帕替尼、阿布昔替尼)、口服JAK1/2抑制剂(巴瑞替尼),以及外用芦可替尼、德戈替尼等。然而,JAK抑制剂的应用也面临挑战。美国FDA基于类风湿关节炎研究对所有JAK抑制剂发布黑框警告,提示在老年、吸烟、有心血管或血栓病史等高危人群中存在主要心血管事件、血栓、恶性肿瘤及严重感染风险。尽管特应性皮炎患者中发生率较低,临床仍需谨慎。未来,治疗将朝向更精准、安全、便捷发展。