全球约 5700 万人正遭受阿尔茨海默病(AD)的困扰,作为导致痴呆的首要病因,其核心病理特征之一便是大脑内 β-淀粉样蛋白(Aβ)的异常沉积,这也让靶向清除Aβ成为 AD 治疗最核心的研发方向。
近年来,以仑卡奈单抗为代表的抗Aβ抗体疗法在临床试验中证实,降低脑内Aβ负荷能够延缓早期 AD 的疾病进展,为患者带来了治疗希望,但这类疗法始终无法绕开关键的安全性难题——治疗常引发患者脑内炎症、淀粉样蛋白相关成像异常(ARIA)、脑微出血等严重不良反应,而降低副作用的调整往往又会伴随治疗效果的折损,成为 AD 抗体疗法临床应用的核心瓶颈。
2026 年 4 月,国际顶级期刊Cell发表了中国科学院动物研究所李伟、胡宝洋、周琪团队的重磅研究成果,研究团队开发出下一代胞外靶向蛋白降解(eTPD)平台——合成多肽编程的溶酶体靶向嵌合体(synthetic peptide-programmed lysosome-targeting chimeras,SPYTACs),凭借全合成双特异性多肽的独特设计,不仅实现了外周与中枢神经系统的协同Aβ高效降解,更从根本上规避了传统抗体疗法的核心安全风险,为 AD 治疗带来了全新的范式。

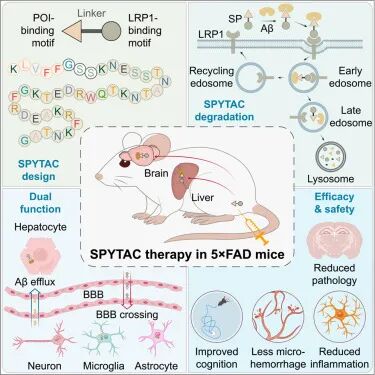
SPYTACs 的核心设计遵循了高度模块化的合成逻辑,其本质是一条人工合成的双特异性多肽,由三个核心功能单元构成:N 端的靶标蛋白结合基序、中间保证结构柔性的 GSS 连接子,以及 C 端的溶酶体转运受体结合基序。
针对 AD 的治疗需求,研究团队最终筛选出最优的 SPAβ-1 分子,其 N 端采用 KLVFF 五肽作为Aβ结合基序,该序列能够精准靶向Aβ自组装的疏水核心,对 β 折叠富集的Aβ纤维、寡聚体展现出远高于单体的结合亲和力,同时还能无差别识别Aβ₄₀与Aβ₄₂两种核心病理亚型,突破了部分抗体仅能靶向单一Aβ形态的局限;C 端则选择了低密度脂蛋白受体相关蛋白 1(LRP1)的靶向肽段,LRP1不仅在肝脏、大脑血管内皮细胞、神经元、胶质细胞中广泛表达,具备天然的组成型循环特性,能够介导配体的网格蛋白依赖型内吞与溶酶体靶向转运,还能直接介导分子跨血脑屏障的转胞吞作用,完美解决了传统 eTPD 药物难以穿透血脑屏障的行业痛点。
通过双特异性的结构设计,SPYTACs 就像一座精准的 “分子桥梁”,一端牢牢抓住致病性Aβ,另一端锚定细胞表面的LRP1,快速形成 “LRP1-SPYTACs-Aβ” 三元复合物,启动受体介导的内吞作用,将Aβ精准转运至溶酶体中完成降解。
研究团队通过一系列细胞实验验证了这一机制的可靠性:只有同时具备双结合基序的 SPAβ-1,才能高效介导Aβ的细胞内吞与溶酶体降解,而敲低或敲除LRP1后,这一效应便会完全消失。同时,SPYTACs 的降解过程严格依赖溶酶体与自噬溶酶体通路,从分子层面明确了其靶向降解的核心原理。
更重要的是,SPYTACs 展现出了 “外周-中枢” 协同清除Aβ的独特能力:在体内,静脉注射的 SPYTACs 主要富集于肝脏,通过肝细胞表面的LRP1高效捕获并降解血液中的Aβ,打破外周与中枢的Aβ动态平衡,间接促进脑内Aβ向外周排出。同时,它还能借助脑血管内皮细胞的LRP1介导跨细胞转运,成功穿透血脑屏障进入脑实质,直接靶向大脑皮层、海马体等核心脑区的淀粉样斑块,推动斑块内Aβ进入溶酶体降解,实现对脑内病理蛋白的直接清除。
在 5×FAD AD 模型小鼠的体内实验中,SPYTACs 展现出了优异的治疗效果,且在疾病的前驱期与症状期均能发挥稳定的治疗作用。针对 5 月龄的前驱期模型小鼠,连续 30 天的每日腹腔注射 SPYTACs 治疗,可使小鼠血浆总Aβ水平降低约 50%,效果显著优于同期的仑卡奈单抗治疗组;在大脑中,SPYTACs 能使小鼠海马体、皮层的淀粉样斑块数量与面积平均减少 40% 以上,不仅降低了可溶性Aβ水平,还能有效清除甲酸溶解的不溶性纤维状Aβ,而同期的仑卡奈单抗仅能降低可溶性Aβ₄₀,对不溶性病理聚集体的清除效果有限。
更关键的是,SPYTACs 治疗显著缓解了模型小鼠的神经元变性,保护了海马体神经元的树突棘密度,逆转了 AD 特征性的突触丢失;在行为学实验中,经 SPYTACs 治疗的小鼠在莫里斯水迷宫、新物体识别测试中均表现出显著改善的空间学习能力、记忆巩固能力与短期识别记忆,认知功能的恢复效果与仑卡奈单抗相当。
针对 9 月龄、已出现明显 AD 病理与认知障碍的症状期模型小鼠,SPYTACs 治疗依然能有效降低脑内Aβ负荷,减少斑块沉积,缓解神经元损伤与突触丢失,同时在水迷宫、Y 迷宫、新物体识别测试中显著逆转小鼠的认知功能缺陷,证实了其在 AD 进展不同阶段的治疗潜力。
相较于传统的抗体疗法,SPYTACs 最具突破性的价值,在于其彻底解决了抗体治疗的核心安全隐患。传统抗Aβ抗体的 Fc 段会结合免疫细胞的 Fc 受体,引发过度的炎症激活、小胶质细胞的非特异性吞噬,还会加重脑淀粉样血管病(CAA),诱发脑微出血,这也是 ARIA 等不良反应的核心成因。而 SPYTACs 作为全合成多肽,完全不含 Fc 段,从结构根源上规避了 Fc 受体介导的免疫激活风险。
实验结果显示,SPYTACs 治疗不会像仑卡奈单抗一样加重模型小鼠的脑血管周围Aβ沉积与 CAA,治疗后的小鼠脑内微出血水平与空白对照组无差异,而仑卡奈单抗治疗组的脑微出血发生率显著升高;同时,SPYTACs 治疗显著降低了小鼠脑内肿瘤坏死因子(TNF)、白细胞介素- 6(IL-6)等促炎因子的水平,而仑卡奈单抗治疗组则出现了明显的炎症因子升高。
通过海马体组织的单细胞测序,研究团队进一步发现,SPYTACs 治疗能够抑制小胶质细胞与星形胶质细胞的病理性激活,推动其向神经保护型的表型转化,下调炎症相关的 NF-κB、炎症小体信号通路;而仑卡奈单抗治疗则会加剧胶质细胞的促炎激活,上调疾病相关的炎症基因表达,这也解释了两种疗法在安全性上的巨大差异。此外,长期给药的安全性评估显示,SPYTACs 治疗不会对小鼠的肝脏、肾脏、心脏、肺等重要脏器造成毒性,小鼠体重、肝功能指标均无异常,展现出了极佳的体内安全性。
除了在 AD 治疗中的亮眼表现,SPYTACs 更是一个具备高度可编程性与通用性的胞外蛋白降解平台。其模块化的设计让靶点替换变得极为简单,只需更换 N 端的靶标结合基序,就能精准靶向不同的致病蛋白,研究团队通过替换 Myc 标签结合序列,成功实现了对 Myc 标签抗体的靶向溶酶体降解,直接验证了这一平台的可编程性。这意味着,除了Aβ,SPYTACs 还能被设计用于靶向 AD 的另一个核心致病蛋白 Tau 蛋白,以及帕金森病相关的 α- 突触核蛋白、渐冻症相关的 TDP-43 等多种神经退行性疾病的致病蛋白,甚至能拓展到胞外致病蛋白驱动的癌症等其他疾病领域。同时,全合成多肽的特性让 SPYTACs 相较于抗体、融合蛋白类降解剂,具备设计合成更简单、规模化生产成本更低、血脑屏障穿透性更优的天然优势,其基因可编码性还能让其进一步与细胞治疗、基因治疗技术结合,拓展出更丰富的治疗形式。
当然,这项研究也存在需要进一步优化的方向,比如未修饰的多肽在体内存在快速清除的问题,目前需要高频给药来维持治疗效果,未来研究团队将通过 D 型氨基酸替换、多肽环化、 锚定肽修饰等方式,优化 SPYTACs 的体内稳定性与半衰期,同时开展更长期的药效与安全性研究,推动这一技术向临床转化。
总体而言,这项来自中国科学家的原创研究,不仅开发出了一种兼具高效性与安全性的 AD 全新治疗策略,更建立了基于合成多肽的胞外靶向蛋白降解新范式,突破了现有 eTPD 技术难以穿透血脑屏障的核心瓶颈,为阿尔茨海默病,乃至所有致病蛋白异常聚集驱动的疾病,开辟了一条全新的治疗道路。



 VIP复盘网
VIP复盘网
