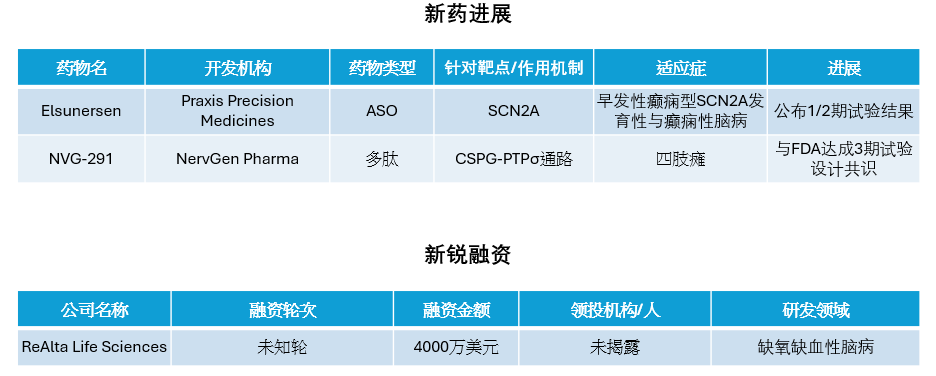
近期,全球多肽和寡核苷酸(TIDES)领域迎来系列进展。NervGen Pharma于近日针对其在研多肽疗法NVG-291用于治疗慢性四肢瘫痪患者的3期试验设计达成共识。Praxis Precision Medicines旗下反义寡核苷酸(ASO)疗法elsunersen在临床1/2期试验当中,使早发性癫痫型SCN2A发育性与癫痫性脑病(SCN2A-DEE)儿童患者的癫痫发作频率较基线降低77%。本文将节选其中部分重要进展做简单介绍,仅供读者参阅。
NVG-291:与FDA达成关键3期试验设计共识
NervGen Pharma近日宣布,公司已与美国FDA完成针对其在研疗法NVG-291的2期临床试验结束会议(EOP2),并就关键性3期注册研究RESTORE的设计方案达成一致。RESTORE是一项为期16周的注册性研究,旨在评估NVG-291在慢性四肢瘫痪患者中的治疗效果。根据双方达成的共识,该研究的主要终点将为第12周时GRASSP定量抓握能力相对于基线的变化,这一经验证的功能性终点主要用于评估患者精细手部运动能力的改善,而手部功能恢复被认为是四肢瘫痪患者最优先关注的功能领域之一。
在次要终点方面,研究还将纳入患者整体改善印象评分(PGIC)和临床医生整体改善印象评分(CGIC),并通过盲法定性访谈进一步评估NVG-291治疗所带来的临床意义。公司表示,RESTORE研究目前正在推进启动准备工作,预计将在2026年年中正式启动。NVG-291是NervGen Pharma的主打在研疗法,为一种皮下注射给药的神经修复多肽,旨在靶向抑制性CSPG-PTPσ信号通路。此前在1b/2a期CONNECT SCI研究中,该疗法已显示出改善慢性四肢瘫痪患者功能、独立生活能力及生活质量的潜力。
Elsunersen:公布1/2期临床试验数据
Praxis Precision Medicines今日宣布,其在研疗法elsunersen在EMBRAVE临床1/2期试验A部分中取得积极结果。该研究在早发性癫痫型SCN2A发育性与癫痫性脑病儿童患者中开展。Elsunersen是一种反义寡核苷酸疗法,旨在选择性降低SCN2A基因表达,从而直接靶向早发性癫痫型SCN2A-DEE的致病机制,用于治疗携带SCN2A功能获得性突变患者的癫痫发作及其他相关症状。

研究结果显示,在疗效方面,与安慰剂相比,elsunersen治疗使患者癫痫发作频率较基线降低77%(p=0.015,95% CI:33–92)。同时,57%的患者实现了至少连续28天无癫痫发作。疗效在开放标签延长期(OLE)中可持续长达一年。此外,与安慰剂组未观察到改善相比,所有接受elsunersen治疗的患者在睡眠、运动功能、肌张力、注意力或神经精神运动发育等指标上均出现改善。在安全性方面,elsunersen整体耐受性良好。
ReAlta Life Sciences:完成4000万美元融资
ReAlta Life Sciences近日宣布完成一笔超额认购的4000万美元融资,使公司累计融资总额超过1.5亿美元。公司表示,本轮融资所得资金将主要用于推进其主打在研疗法pegtarazimod的关键临床与监管里程碑。根据新闻稿,pegtarazimod有望成为首个治疗缺氧缺血性脑病(HIE)的疗法。接下来,公司计划完成正在进行的2期STAR临床试验,并将迎来顶线数据公布,同时公司还计划与美国FDA举行2期临床试验结束会议。
一体化平台助力寡核苷酸药物开发
在寡核苷酸(Oligo)药物研发快速发展的背景下,从序列设计到生产制造的一体化能力对于提升研发效率与成功率至关重要。药明康德依托多业务平台协同优势,构建了覆盖药物发现、机制研究、药代动力学评价以及开发与生产的一体化寡核苷酸研发体系,为合作伙伴提供端到端支持。
药明康德生物学业务平台(WuXi Biology)建立了覆盖设计、筛选、评价与转化研究的一体化Oligo药物发现平台,可为合作伙伴提供端到端的寡核苷酸研发支持。平台依托自主建立的in silico序列设计体系,综合考虑脱靶风险、跨物种活性及序列特征等多维参数,实现候选Oligo的高效设计与优选;结合超过1500种细胞资源及多类型细胞模型开展高通量体外筛选与功能评估,快速识别具有高敲降效率和良好特异性的候选分子。在安全性与机制研究方面,平台整合RNA转录组分析、免疫原性与细胞毒性检测,实现对脱靶效应与潜在安全风险的系统评估。在递送技术方面,除肝靶向GalNAc策略外,平台还支持肝外递送工具的发现,包括抗体和多肽等配体,并通过优化偶联位点与DAR提升递送效率。通过跨学科整合与标准化流程,WuXi Biology将Oligo设计与优化、递送、安全性评估及药效评价紧密衔接,有效降低早期研发风险,加速创新寡核苷酸疗法迈向临床阶段。
针对寡核苷酸药物在体内主要由核酸内切酶与外切酶介导降解、其代谢路径与传统小分子显著不同的特点,药明康德DMPK团队建立了系统化的体外代谢研究平台,通过多模型协同策略对寡核苷酸药物的稳定性与降解行为进行全面评估,为候选分子的优化与临床前决策提供关键数据支持。依托多年寡核苷酸DMPK研究经验,团队构建了覆盖多种生物基质的体外稳定性模型体系,包括血浆、血清、肝脏与肾脏S9组分、组织匀浆、肝细胞及溶酶体等研究系统,可根据分子结构特点与作用靶点选择合适模型开展代谢稳定性研究,从而更真实地模拟体内降解环境。通过比较不同模型中的代谢速率与代谢产物形成情况,团队能够系统解析寡核苷酸在循环系统与靶组织中的清除路径,并支持跨物种差异评估,提高体外结果对体内行为的预测能力。同时,通过对孵育体系、基质选择及实验参数的持续优化,团队提升了模型稳定性与数据一致性,使体外研究能够更准确反映真实代谢特征,从而在早期研发阶段识别代谢风险、指导分子修饰策略,并支持后续药代与安全性研究,为寡核苷酸药物从发现阶段迈向临床开发提供重要科学依据。
药明康德旗下专注于寡核苷酸、多肽及相关化学偶联药物的CRDMO平台WuXi TIDES,也为包括RNAi在内的寡核苷酸原料药和制剂提供从药物发现到商业化生产的一体化服务。其寡核苷酸发现与合成服务支持高通量库合成和定制合成,涵盖多种类型的寡核苷酸及其单体、连接子、配体和偶联物。依托充足的产能与成熟的商业化经验,平台能够将生产规模快速扩展至不同阶段所需水平,满足从临床前研究、临床开发到商业化生产的多样化需求。WuXi TIDES同时提供多种剂型和灌装形式的制剂开发与生产服务,并在同一质量体系下为原料药和制剂提供一体化分析支持以及全面的CMC申报资料撰写服务,从而帮助合作伙伴加速推动寡核苷酸创新疗法迈向市场。



 VIP复盘网
VIP复盘网
