近日,中美博弈,川普的关税大棒再次挥向医药行业。
消息一出,资本市场风声鹤唳,不仅创新药板块应声下跌,CXO行业也集体受挫。然而,抛却恐慌情绪便会发现,这一针对创新药的关税政策,对具有前瞻性全球布局的CXO公司来说,却基本无实质影响。
具体为什么呢?下文从:①中国创新药为什么要出海;② 创新药/专利药/品牌药&仿制药基础知识;③ 我国创新药的出海模式;④ 创新药出海发展历史;⑤ 关税对国内创新药影响有多少;⑥总结与展望;等六个维度来剖析。

一、中国创新药为什么要出海
不出海,便出局。中国创新药近年来加速“出海”,这并非简单的商业选择,而是行业发展到一定阶段的必然战略,背后既有国内市场结构变化的驱动,也离不开国际市场需求与政策红利的双重支撑。
1、向蓝海市场进军,从内卷到破局
国内创新药赛道的白热化竞争迫使企业寻求海外增量空间。以PD-1抑制剂为例,国内已有15款同类药物获批上市,价格从上市初期的年治疗费用10万元以上降至不足2万元。
恒瑞医药的卡瑞利珠单抗在国内医保谈判中降价85%后,2023年国内销售额同比下滑28%,而其通过海外授权(如与德国默克集团合作)获得的首付款及里程碑收入达6亿美元。
这种“以海外养国内”的策略成为行业共识——2024年国内药企达成94笔License-out交易,总金额519亿美元,同比增长24.5%,其中恒瑞医药单年完成5笔授权,涉及GLP-1、ADC等前沿领域,潜在总交易额超100亿美元。
2、追求更大的利润池
出海,意味着更大的市场和回报,创新药研发具有 “高投入、长周期、高风险” 的特点,仅靠国内市场难以收回成本并获得持续发展的利润。
通过对外授权(License-out)或自主在海外上市,药企能够进入欧美等支付能力更强的成熟市场,以及人口众多、增长潜力巨大的新兴市场,从而显著提升产品的销售额峰值和生命周期价值。
2025年上半年,中国创新药对外授权总金额已超过660亿美元,超过2024年全年的519亿美元。例如,恒瑞医药在2025年已达成多笔重磅交易,累计潜在交易总额突破150亿美元。
3、研发实力获国际认可,从“跟跑”到“并跑”
中国药企的原创能力和临床试验数据质量已达到国际水准,这是出海的前提。 截至2025年一季度,全球32% 的生物科技类授权合作发生在中国。复宏汉霖的地舒单抗注射液在2025年9月同时获得美国FDA和欧盟的上市批准。
另外,在ADC(抗体偶联药物)、双抗等新兴技术前沿领域,中国研发已占据全球重要地位。恒瑞医药的HER2 ADC药物SHR-A1811成功授权出海,正是其ADC平台技术积累超过10年的成果体现。
4、深度参与全球创新分工
出海不再是单一的产品授权,而是通过多元化的深度合作,参与甚至主导全球医药创新。
比如,百奥赛图,不再仅仅出售个别具体药物,而是通过其基因编辑动物模型和抗体发现平台,已累计签署超280项全球合作授权协议,成为全球药企的研发“基础设施”。
另外,甘李药业以技术换市场,通过技术转移帮助巴西建立本土胰岛素生产能力,不仅获得了长期稳定的订单(金额预计不低于30亿元人民币),更深度融入了当地的公共卫生体系,打破了跨国药企的长期垄断。这种模式开创了“技术输出-本地生产-全球供应”的新范式。

二、创新药/专利药/品牌药&仿制药基础知识
1、什么是创新药
创新药(First-in-Class)是指基于全新作用机制、分子实体或治疗方法开发且具有明确临床价值,在全球未上市的药品。
从研发层面看,与传统仿制药(Me-too)复制已有药物或改良药(Me-better)对现有药物进行优化有本质的不同,创新药通常涉及靶向治疗、基因编辑、免疫疗法等前沿技术,历经靶点发现与验证、先导化合物筛选、临床前研究、I—III期临床试验等漫长过程。
其高投入、长周期和高风险的现实被业界形象地用3个“10”来形容,即10亿美元投入、10年研发周期以及10%的成功概率,真正代表着医药领域从“0到1”的原始创新。
总之,创新药,本质上即原研药或专利药、品牌药,是一个相对于仿制药的概念
2、什么是专利药/品牌药
原研药,英文 Innovator Drug,又称专利药或品牌药,是指由制药公司自主研发并首次上市的药物。其研发过程复杂且耗时,通常需要10-15年的时间,涉及成千上万种化合物的筛选、临床前和临床试验(包括Ⅰ至Ⅳ期),以及上市后的长期监测。
3、仿制药概念
仿制药,英文 Generic Drug,是在原研药专利保护期结束后,其他制药企业通过逆向工程复制原研药的主要分子结构进行生产的药物。仿制药的研发虽以原研药为参照,但流程并不简单,需建立与原研药等同的质量标准等。并主要通过一致性实验证明其与原研药在体内吸收速度和程度上一致。
即,仿制药前提是要通过仿制药质量和疗效一致性评价Consistency Evaluation—— 这是我国判断仿制药能否与原研药等效替代的核心标准。
另外,国家的药品集采,大都为仿制药,因为国产仿制药由于省去了大量的研发成本,能够以较低的价格参与竞争,入选率很高,2024 年 12 月我国第 10 批药品集中采购中,所有原研药无一中标和入围。
下图:药盒上如有左图所示的蓝色图标,即表示该药品已通过仿制药一致性评价

4、原研药&仿制药区别
原研药和仿制药是生命健康的双引擎,在普通片剂、胶囊剂等简单剂型,可实现与原研药的 “互换使用”;剂型复杂(如缓释片)、生物制剂类(如单抗)仿制药,工艺精细,难度高,药效易受影响,临床效果一般。
专利药或品牌药与仿制药在研发过程、价格、疗效与安全性、生产工艺与市场地位等方面存在一定差异,如下表:

三、我国创新药的出海模式
我国创新药的主要有4种出海模式:自主出海、联手出海、借船出海、NewCo,每种模式均赋予了企业不同程度的海外市场研发、商业化及整体战略的话语权。
1、四种模式分析
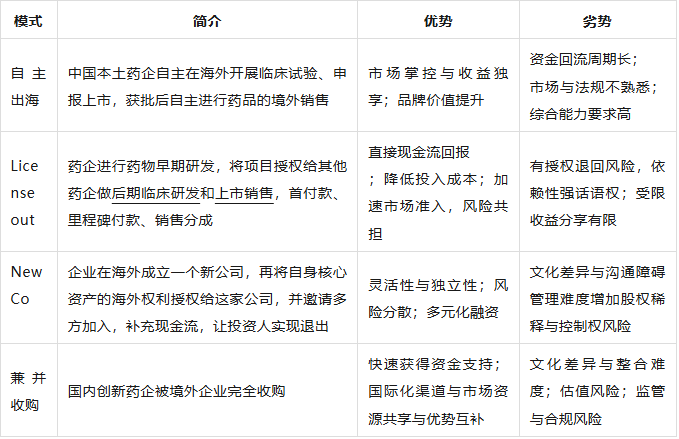
自主出海是指国内药企自主开拓国际市场,在海外开展临床试验和提交新药上市申请,自主搭建商业化团队进行海外销售,适合资金实力雄厚、研发能力强且拥有丰富海外运营和风险管理经验的大型药企。
其优势是:企业能够独立掌握海外研发进度,独享商业化运营收益;劣势是:资金回流周期长、国际监管法规不熟悉等沉没成本和失败风险。如信达生物信迪利单抗、万春药业普那布林由于缺少美国患者临床试验数据、不符合FDA监管要求等导致出海失利。
自主出海的典型案例是:2019年11月,百济神州自主研发的BTK抑制剂泽布替尼以“突破性疗法”成功获得美国FDA批准上市,实现本土新药自主出海“零的突破”。2023年泽布替尼全年收入首次突破10亿美元大关,成为首款国产“重磅炸弹”药物,为我国创新药自主出海树立标杆。
(2)License-out(对外授权)--当前为主流
license-out,对外授权,也叫授权合作,是本土企业将药物研发、临床或商业化权益授权给海外企业,获取首付款、按里程碑模式获得各阶段临床成果、和销售分成的模式。
license-out是目前中国药企出海最为主流的选择。其核心在于借助外部力量,如国际制药巨头、跨国医药企业或专业医药投资机构的资源与经验,实现产品的海外推广与商业化。其中,跨国药企MNC (Multi - National Company)实力买家占据跨境License-out交易卖家的绝大多数,仅BioNTech一家为新冠疫苗起家的转型企业。
此模式显著降低了中国药企在国际化初期的投入门槛,尤其适合那些资源相对有限、国际化经验尚浅的企业。通过合作,企业能够加速产品进入国际市场,缩短市场渗透周期。
但其弊端是:本土药企失去产品研发和商业化运营自主权,面临海外监管机构质疑、临床试验数据缺乏、双方合作取消等诸多不可控风险导致出海受阻,复创医药、基石药业、诺诚建华、加科思等在出海过程中均被退回。
其典型代表是:2023年11月,和黄医药呋喹替尼获得FDA批准上市,为创新药借船出海提供新样本。2023年,和黄医药与武田制药达成呋喹替尼全球独家许可协议,武田制药获得在中国大陆、香港和澳门以外地区开发和商业化独家权利,和黄医药将累计获得总额11.3亿美元交易款。借助武田制药全球销售网络和资源,呋喹替尼快速打入国际市场。
(3)NewCo--新趋势
本土药企与海外资本(基金)共同成立新公司,将特定管线资产的海外权益授权给新公司,邀请多方资本参与提供资金支持,并为投资人提供退出机制,企业获股权和收益。
“NewCo模式”在海外跨国制药企业中不乏先例,此模式具有高度的灵活性和独立性,能够迅速适应不同海外市场的法规、文化和消费者需求。同时通过引入多元化的投资者和合作伙伴,不仅为 NewCo 提供了充足的现金流支持,还促进了资源的有效整合与优化配置。原始企业则保留对 NewCo 的部分股权,以确保长期利益绑定,实现与新公司的共同成长和互利共赢。
劣势是由于规模和投资者结构的复杂化,NewCo的管理难度也会相应增加,需要投入更多资源和精力来维护各方利益平衡,且原始企业可能需要不断稀释自身股权,从而面临控制权减弱的风险。
典型代表是:2024年,恒瑞医药转变出海战略,将具有自主知识产权的GLP-1产品组合有偿许可给海外新公司Hercules,率先解锁NewCo新模式。Hercules是恒瑞医药与贝恩资本生命科学基金联合Atas Ventures、RTW资本等共同设立。
下图:NewCo模式出海代表:

(4)并购整合(M&A)
M&A,mergers and acquisitions,并购整合,即企业被海外药企或投资方收购,借助对方资源拓展海外市场。被外国公司兼并收购(M&A)为国内创新药企提供了新的退出路径和成长机会,也能够帮助其快速实现国际化转型。
近几年来,中国创新药企被外国公司并购数量和总金额都在逐年上升,仅2024年H1披露的收购总金额相较于2023年全年的数据已经实现了29.15%的增长,这一现象鲜明地反映出 MNC 对中国创新药企研发实力的广泛认可,并且,中国创新药企在当前估值上展现出的“高性价比”特征。
国内被收购的典型代表是亘喜生物。23年12月26日,阿斯利康宣布,以约12亿美元的总价收购亘喜生物,该总价较之亘喜生物在23年12月22日的美股收盘价溢价86% 。收购完成后,其为阿斯利康的全资子公司,在中国和美国开展业务。
2、23/24/25年出海比较
如果2023年是出海“元年”,2024年是“加速年”,那么从2025年展现的态势来看,这一年可以定义为 “升级年”或 “成果年” 。中国药企的出海进程实现了从量变到质变的飞跃,展现出更深、更广、更成熟的新特征。目前中国创新药出海之路多种模式并驾齐驱,共同推动国产创新药走向国际市场。

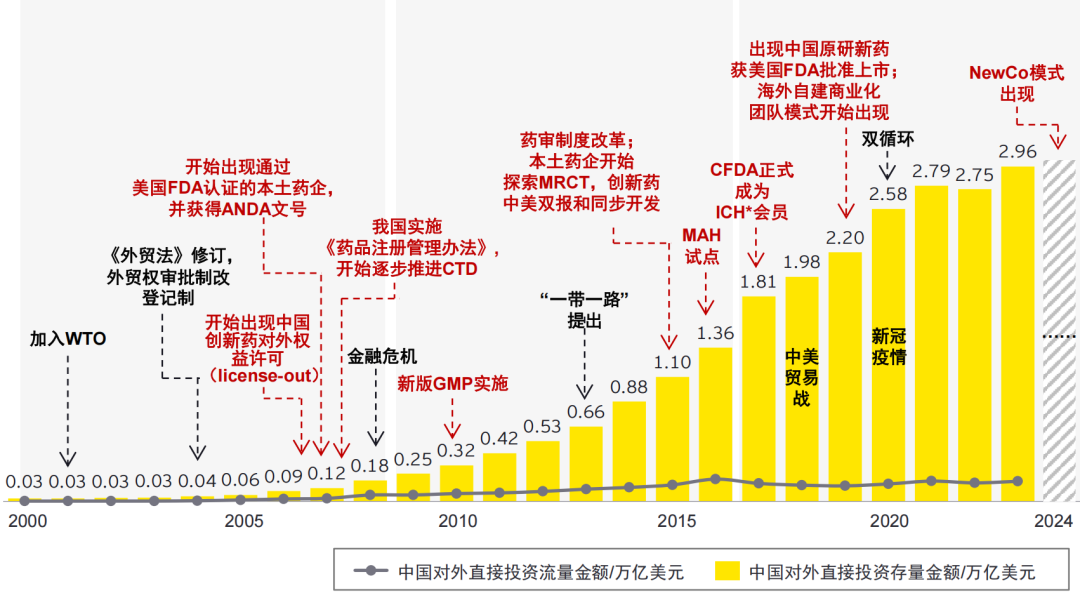
四、创新药出海发展历史
中国创新药出海历经多阶段演进,从早期供应链出海逐步迈向自主创新国际化,以下是关键发展历程:
1、探索阶段:原料药与仿制药出海(2000-2010年)
此阶段以低成本供应链为核心竞争力,为创新药出海积累基础。2000年后中国加入WTO,原料药凭借成本优势快速占据国际市场。
1992年海正药业打开国际中高端原料药市场,中国现承担全球近1/3原料供给。
2007年美罗药业二甲双胍片剂出口澳洲,实现中国处方药出口“零的突破”,华海药业奈韦拉平成为首个通过FDA认证的国产制剂。
2、起步阶段:创新药出海突破(2010-2020年)
此阶段政策与模式双重驱动,创新药出海实现从0到1的跨越。
2010年后仿制药通过GMP、FDA等国际认证,逐步进入欧美高壁垒市场。2017年中国加入ICH,创新药研发与国际标准接轨,IND申报数量大幅增长。
2019年百济神州泽布替尼获FDA批准上市,成为首款中国自主研发并在美上市的抗癌新药,实现原研新药出海“零的突破”。
2020年为出海首年,License-out对外授权,项目数量猛增至39款,创新药开始通过国际合作快速打开海外市场。
3、爆发阶段:规模化与多元化(2021年至今)
2021年,艾力斯与Arrivent达成的伏美替尼海外授权合作被视为国内首个典型NewCo交易。此后,康方生物、恒瑞医药等企业纷纷跟进,2024年成为NewCo模式在国内爆发式增长的年份。
2023年License-out案例达58个,交易金额突破465亿美元,ADC药物等新兴赛道成为出海新热点。2024年中国创新药交易总额占全球比重升至30.6%,2025年上半年占比达47%,自主研发实力获国际认可。
2025年君实生物特瑞普利单抗成为首个获FDA批准的中国自主研发创新生物药,本土药企开始探索自主商业化与本地化运营。

五、关税对国内创新药影响有多少?
一言以蔽之:美国对品牌药和专利药加征100%关税的政策,对绝大多数中国领先药企的直接影响非常有限。这主要得益于中国药企已经成熟的出海策略巧妙规避了关税风险。
1、短期中国药企为何能“免疫”
(1)“美国生产、美国销售”的本地化模式:豁免条款
关税政策明确对已在美国启动建厂或在建项目的企业豁免。截至2025年,百济神州已投资8亿美元建成新泽西州生物制药生产基地,药明康德计划于2026年投产美国米德尔顿基地,恒瑞医药等企业也在评估本地化生产可行性。这类企业的在美销售将不受关税影响,且未来产能扩张可进一步巩固市场地位。
(2)主流的“授权出海”License-out模式:
我国创新药出海模式以知识产权授权为主,这是目前最主流的出海方式。中国药企将产品的海外权益授权给跨国药企(如辉瑞、诺华等),由后者负责后续的生产、临床、注册、商业推广以及承担可能的关税成本。在这种模式下,中国药企主要收取首付款、里程碑付款并享受销售分成,不直接涉及药品的跨境出口,从而建立起一道“防火墙”。
(3)精准的差异化定位:
很多中国药企对美出口的业务重点是仿制药和原料药(占比70%),而品牌创新药出口极少。而这两类产品被明确排除在此次关税政策之外。
2024年,中国对美西药出口额为64.25亿美元,仅占美国进口总额的2.7%,其中品牌药占比不足5%。即使关税生效,受影响的中国创新药品种仍局限于少数已在美自主销售的产品,如百济神州的PD-1抑制剂替雷利珠单抗,但该公司通过自建美国生产基地已实现本地化供应。
另外,像华海药业这类以仿制药出口为主的公司可以明确表示“影响有限”。
2、长期潜在挑战
尽管短期直接冲击很小,但这项政策是一个强烈的信号,预示着未来全球医药市场的竞争规则可能发生变化。
(1)加速“全球本地化”战略:
政策会倒逼全球药企(包括中国药企的合作伙伴)更加强调供应链的本地化。这将促使中国药企在未来的对外授权或自主出海规划中,将生产基地的全球化布局作为更核心的考量。
(2) “技术输出”价值凸显:
当单纯的药品出口面临更多不确定性时,中国药企在早期研发、临床试验效率(中国临床试验成本较低且患者招募速度快)等方面的优势将更具价值。通过技术平台授权等方式参与全球分工的合作模式可能会更受青睐。
(3)保持对非关税壁垒的警惕:
需要关注美国是否会在未来以“国家安全”等名义,对医药领域的知识产权合作、技术交易设置更严格的审查(例如传闻中CFIUS的审查)或更高的监管费用。持续提升自主创新的质量和全球专利布局是应对一切不确定性的根本。
3、我国不同药企影响情况表
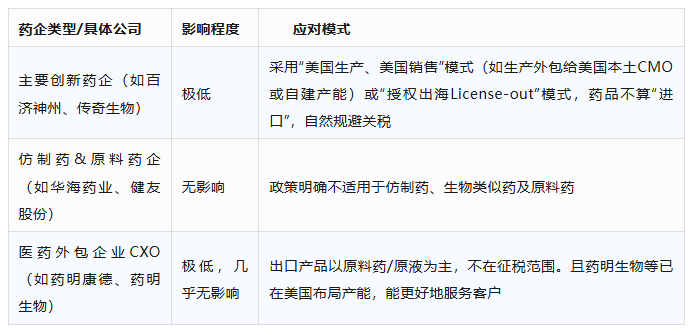
综上,不同于制造业的产业逻辑,关税受上游原材料进口的影响;创新药大部分利润来源是在专利保护下,药品销售的高溢价的,而不是上游原材料的进口,此部分利润占比非常小,而我国的出海是造船出海或授权出海,相当于把整个生产都搬到海外去了。
而此轮的波动,更多是情绪上的感染和影响,先急速的下杀,下杀后都是连续几天比较快速的反弹。究其原因,主要是大家也看明白了,关税最终也不会影响创新药的整个产业趋势。
六、总结与展望
总的来看,这次关税政策对欧洲药企冲击较大,而中国领先的药企凭借其前瞻性的出海策略和业务结构、不可替代的全球供应链韧性,形成了有效的“免疫体系”。
长期而言,它可能会继续推动中国药企的全球化进程从产品出口向更深层次的 产能布局和技术输出升级。
而中国,已经从仿制药的“跟跑者”到创新药的“远航者”。

展望前路,中国创新药需从“单点突围”转向“体系深耕”。锚定全球未满足的医疗需求,在罕见病、代谢疾病等领域打造差异化优势;构建覆盖中美欧的临床研发网络,以符合国际标准的数据,赢得FDA信任。
从“产品出海”到“能力出海”,从“借船远航”到“造船立标”,中国创新药正褪去青涩,在全球医药创新的浪潮中,书写东方原研药的新篇章!



 VIP复盘网
VIP复盘网
