目前,脑机接口(BCI)正处于从“实验室验证”向“规模化商用”跃迁的奇点时刻。在“政策红利 底层技术 多元场景”的三轮驱动下,BCI 赛道正迎来估值重塑。随着规划布局和器械标准的密集落地,行业已进入增长快车道。
目前,产业呈现“双轨并行”态势:
▸非侵入式部分产品已抢滩消费市场,包括康复设备和睡眠辅助设备等。
▸ 侵入式产品在 Neuralink 量产预期及国内临床突破的催化下,正加速跨越临床门槛。
市场层面,目前,我国脑机接口企业总量已突破200家。根据赛迪顾问的研究数据,2024年中国脑机接口市场规模为32.0亿元,增长率为18.8%;预计2028年,中国脑机接口市场规模将达到61.4亿元,2024年至2028年的年复合增长率为17.7%。
随着芯片集成、电极材料及解码算法的迭代,叠加合规化路径的明晰,BCI 产品的商业化“井喷期”已近在咫尺,将加速迎来密集商业化阶段。
脑机接口的分类与“底层逻辑”
简单来说,BCI 是在大脑与外部设备之间搭建的一条“数字直连通路”。它最核心的突破在于:绕过了常规的脊髓和外围神经肌肉组织。这意味着,即使身体的“硬件受损”(如高位截瘫或神经疾病),大脑的指令依然可以通过这道“数字旁路”,直接驱动轮椅、机械臂或是电脑光标。
我们可以将其理解为一场跨越生物界与数字界的“同声传译”:采集信号(感知大脑微弱电波) → 解码转化(算法识别意图) → 执行反馈(驱动设备并给予感知回传)。
脑机接口并不是单一的技术产品,根据信号采集终端与大脑的“亲疏程度”,其技术路径与监管逻辑也截然不同。目前,业界最主流的分类方式是基于植入位置与侵入程度:
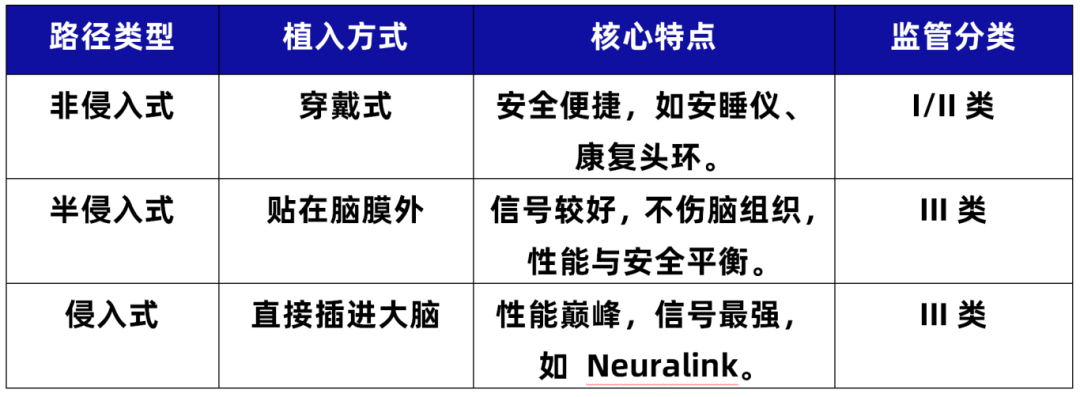
1.国内监管现状概览
目前,中国正以前瞻性布局,快速建立全球领先的BCI标准体系:今年1月1日,我国首个脑机接口医疗器械标准《YY/T 1987-2025 采用脑机接口技术的医疗器械术语》正式实施;同时,测试相关方法的标准《YY/T 1996-2025 采用脑机接口技术的医疗器械 具备闭环功能的植入式神经刺激器 感知与响应性能测试方法》也即将实施。国家药监局近日又批准了《采用脑机接口技术的医疗器械范式设计与应用规范运动功能重建》、《采用脑机接口技术的医疗器械侵入式设备可靠性验证方法》等2项医疗器械行业标准制修订项目立项。旨在解决临床转化中的迫切需求。
中长期目标:政策文件明确了关键技术突破(2027年)和培育全球领先企业(2030年)的阶段性目标。
以下列举的是中国BCI相关的重大监管审批进度:
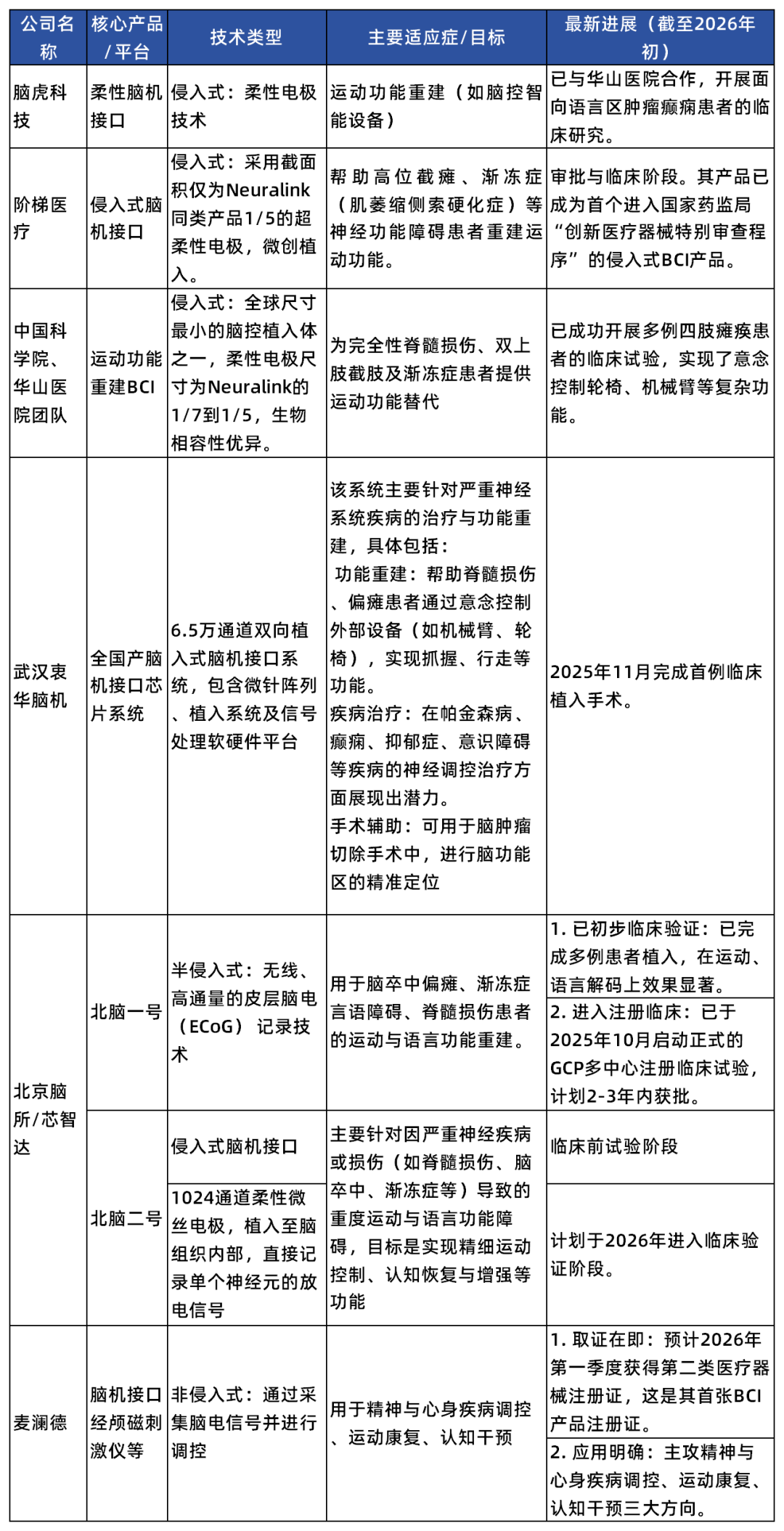
表1: 2025-2026年中国BCI监管进展
2.国际监管现状概览
2.1 美国(FDA):
FDA将BCI设备归类为III类医疗器械(最高风险等级),需要符合下列要求:(1)上市前批准(PMA):具备临床试验数据;(2)临床试验前:需要获得IDE(研究性器械豁免);(3)质量体系:符合21 CFR Part 820要求;(4)上市后监测:持续的长期安全性报告。
植入式BCI需通过严格的研究性器械豁免(IDE) 进行临床试验,才能最终获批上市。FDA意识到脑机接口技术的特殊性,为此发布了专门的技术指南——《用于瘫痪或截肢患者的植入式脑机接口(BCI)设备:非临床测试和临床注意事项》,为IDE申请提供明确的方向。
FDA还通过设立突破性设备计划加速BCI设备的审查。“突破性器械计划” 为符合条件的创新脑机接口提供加速路径。
以下列举的是美国FDA相关的重大审批进度:
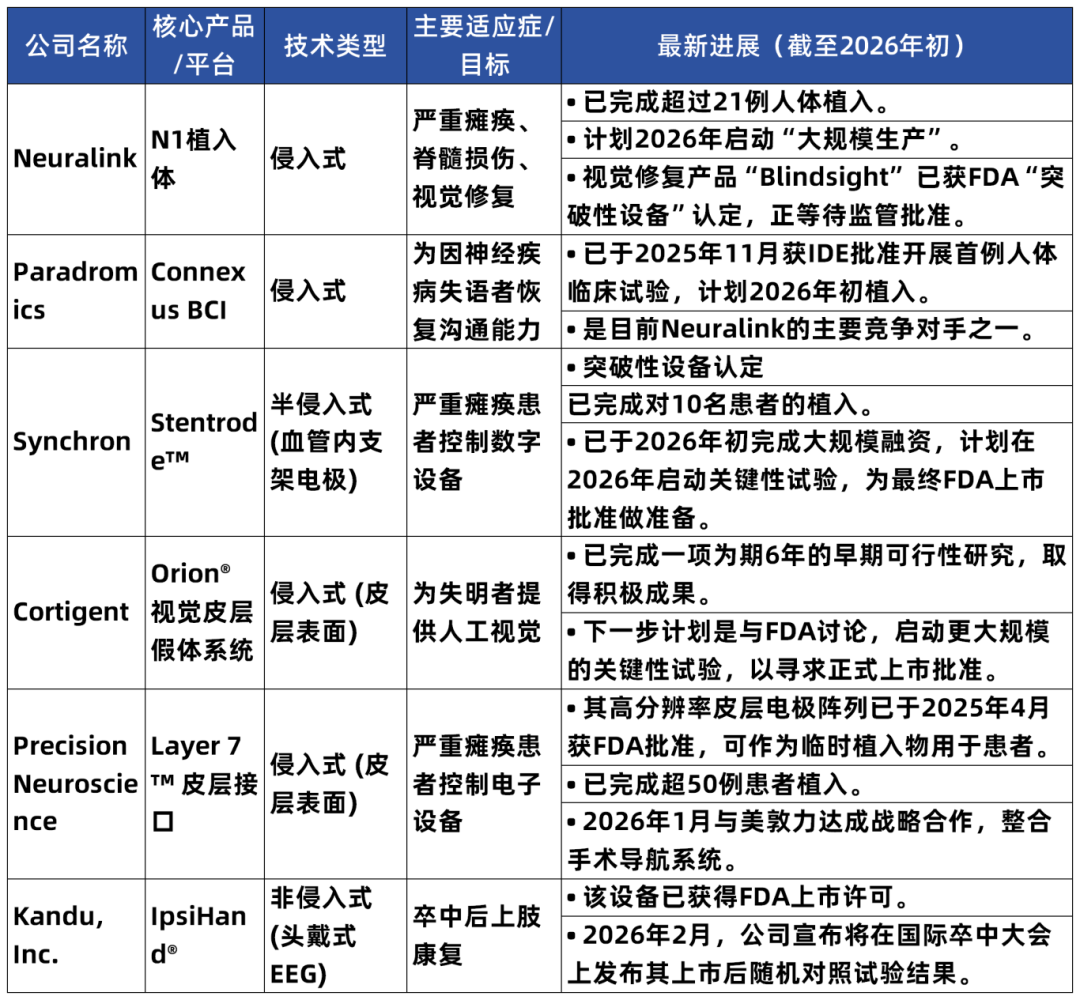
表2: 2025-2026年美国BCI监管进展
2.2 欧盟 (公告机构/各国主管当局):
BCI产品在欧盟需要符合MDR(2017/745)要求,将植入式BCI归为最高风险的III类医疗器械,其临床研究需经成员国主管当局和伦理委员会批准,临床评价的要求包括:临床试验数据或等效临床数据、长期随访数据、真实世界证据;并强调对网络安全、数据保护(GDPR)的严格要求。目前针对BCI监管,欧盟正在制定BCI-specific协调标准,部分欧盟国家提供BCI监管沙盒,并与FDA的监管互认协议进行谈判。
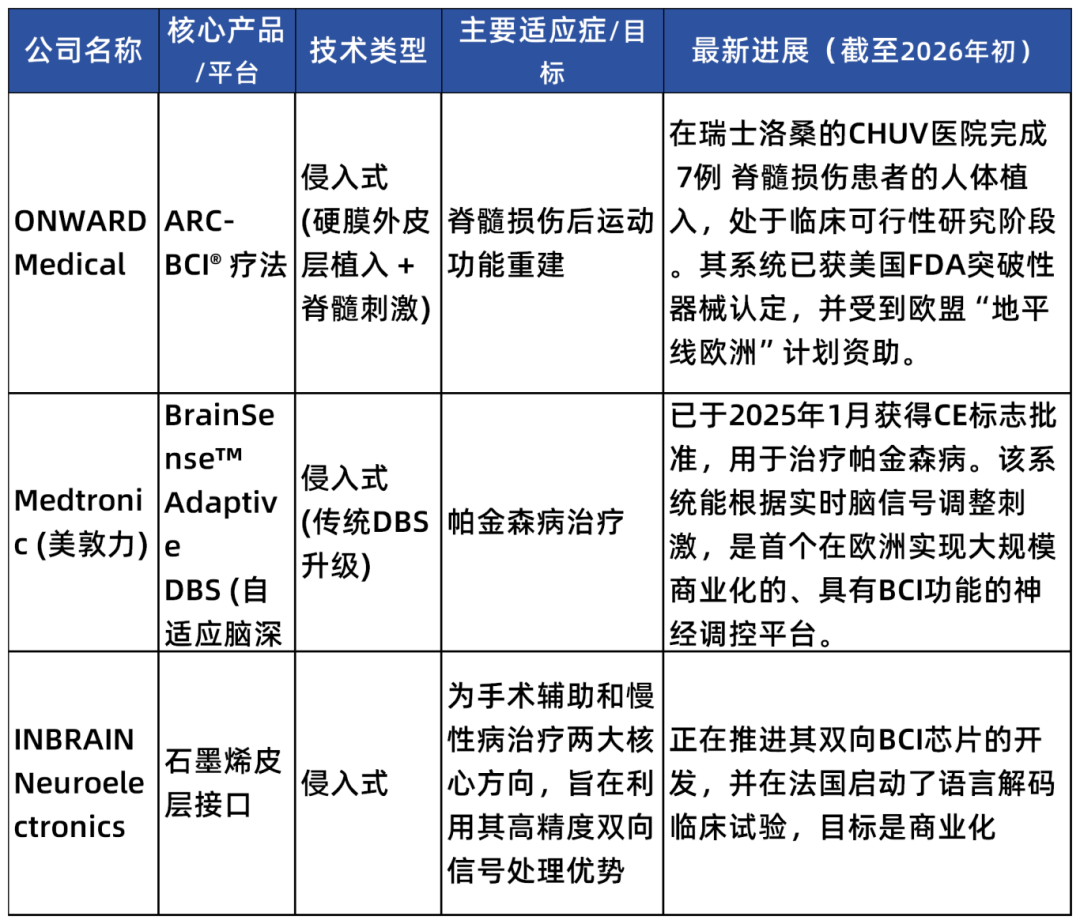
表3: 2025-2026年欧盟BCI监管进展
而在更广泛的消费与健康领域,非侵入式脑机接口正以前所未有的速度走进日常生活。从针对失眠人群的助眠仪,到用于压力管理的神经调制设备,BCI 技术正在情绪调控与人机交互场景中释放巨大潜力。随着 Neuralink 等头部企业迈向商业化量产阶段,国内临床试验也接连取得突破,一个涵盖上游核心器件、中游系统集成到下游多元应用的万亿级产业链版图已清晰可见。
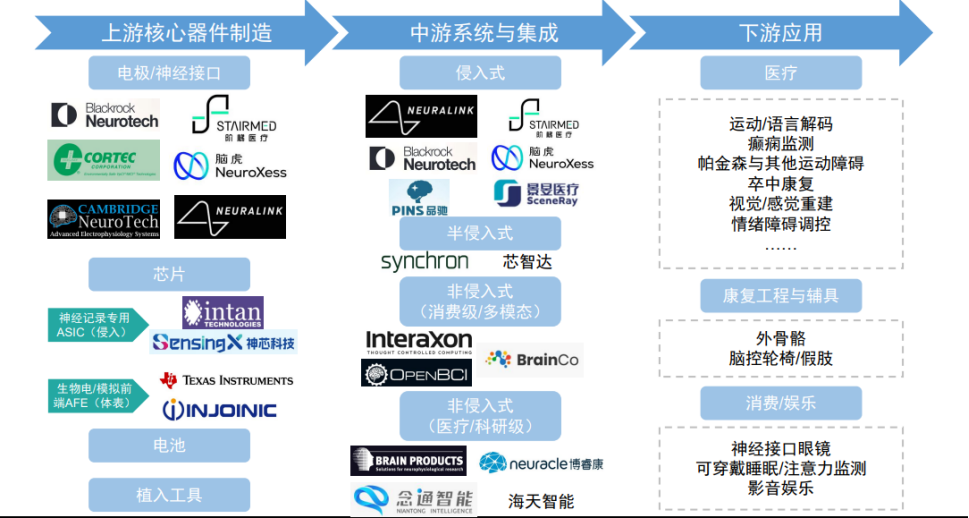
*信息来源:国信证券(脑机接口专题报告——技术突破与商业化共振,关注脑机接口未来产业)
作为中国第三方检测与认证服务的领跑者,CTI华测检测深耕医疗器械领域多年,现已在前沿的脑机接口(BCI)赛道逐渐构建起覆盖全生命周期的“一站式”检测服务体系。我们深知,在这场通向未来的速度竞赛中,技术研发的“天花板”由创新决定,而商业化的“底线”则由安全与质量筑牢。
针对非侵入式脑机接口设备,华测检测依托顶尖的安规及电磁兼容实验室,能够为研发企业提供涵盖 GB 9706.1 等核心标准的精准测试。广州纽维生物学实验室和昆山无源医疗器械实验室可以为产品提供符合GLP体系下的生物学评价。在临床大动物实验上,华测检测昆山生物大动物实验室已成立了脑机专项小组,可高质量完成大部分脑植入手术。
有源医疗器械基本安全和基本性能检测
有源医疗器械电磁兼容检测
BCI相关性能检测
软件测评&网络安全测试
生物学评价
微生物测试
清洗消毒灭菌验证
在脑机接口检测的无人区,华测检测以专项团队为前哨,探索人机融合的下一站,助力更多产品合规上市,共赴科技未来。



 VIP复盘网
VIP复盘网
