遮蔽肽起源于抗体疗法中前药的概念,近年免疫疗法是创新药研发中的热点领域,但是相关的严重免疫不良反应一直是限制免疫疗法应用的限制因素。不少药企都在寻找一种可行的技术,将免疫疗法的副作用控制在最小水平。
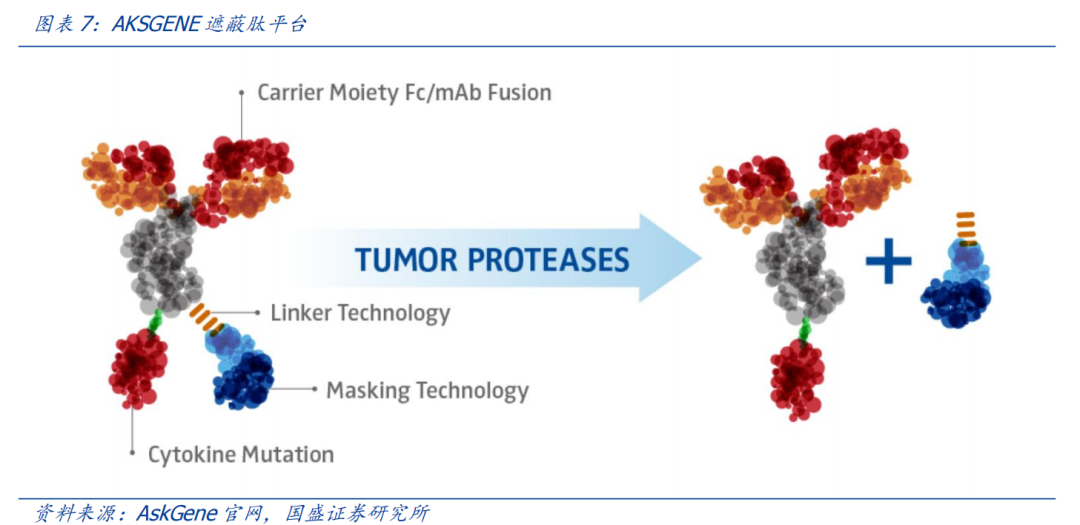
遮蔽肽是一种应对靶向性和非靶向性细胞毒性的解决策略。其结构由三部分组成:一个与抗体轻链N端结合的遮挡肽、一个连接遮挡肽与抗体的蛋白酶可切割接头、一个具有抗癌作用的抗体。
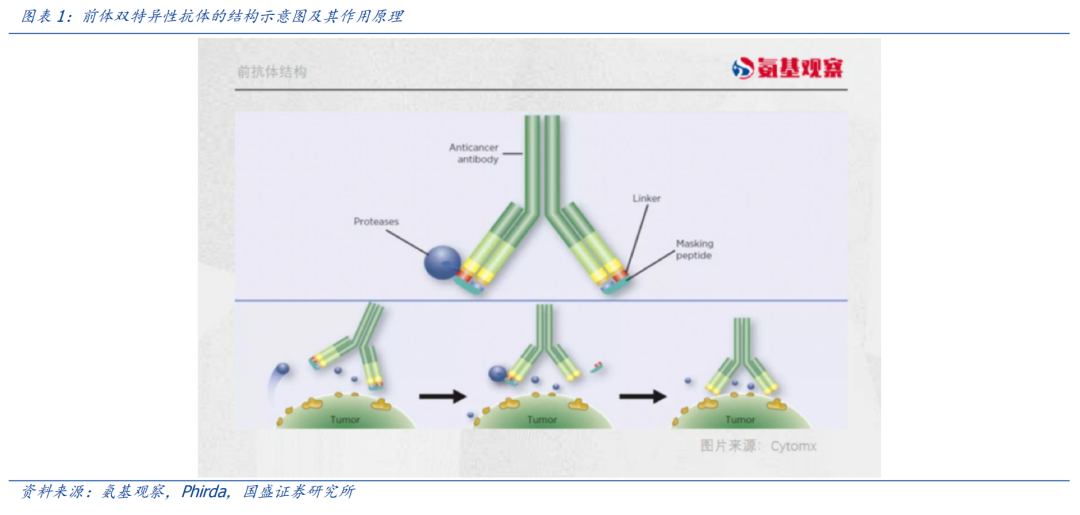
以TCE双抗为例,带有遮蔽肽的TCE双抗,在达到肿瘤特定部位后,在某些酶的作用下进行酶切,去除遮蔽表位的一小段多肽,暴露结合位点,行使双特异性抗体的功能。
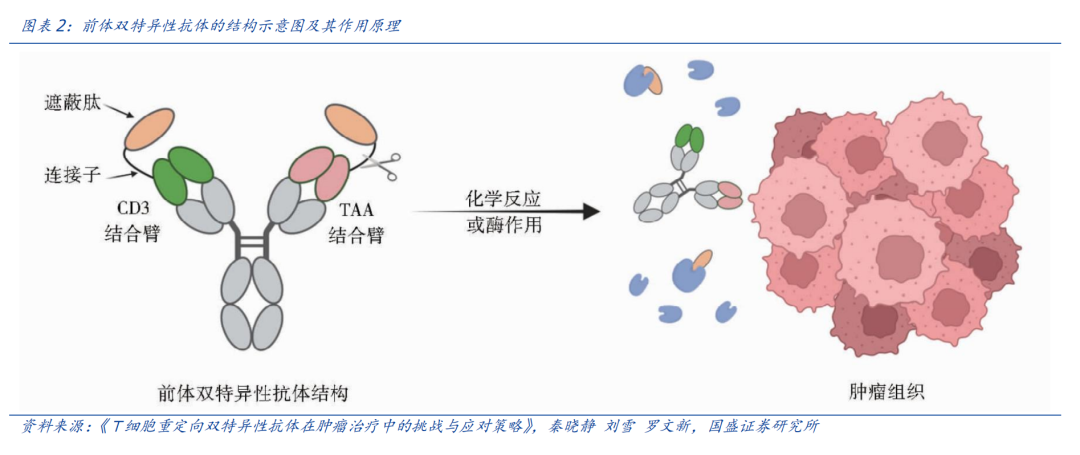
从早期临床结果来看,在文献《Precision-activated T-cell engagers targeting HER2 or EGFR and CD3 mitigate on-target, off-tumor toxicity for immunotherapy in solid tumors》中,XTEN即为用到的遮蔽性多肽,没有经过多肽遮蔽的TCE这里称之为uTCE。如图所示,与未被遮蔽的HER2-uTCE相比,XTEN多肽遮蔽的存在使TCE对HER2的目标亲和力降低了10倍,对CD3的目标亲和力降低了约6倍。
2013年,Cytomx带着前抗体技术Probody正式亮相。看起来,这一技术能够降低抗体类药物的不良反应,拥有极为远大的想象空间:不仅能够增加现有药物的治疗窗,减毒增效;更能给未成药靶点带去成药曙光。
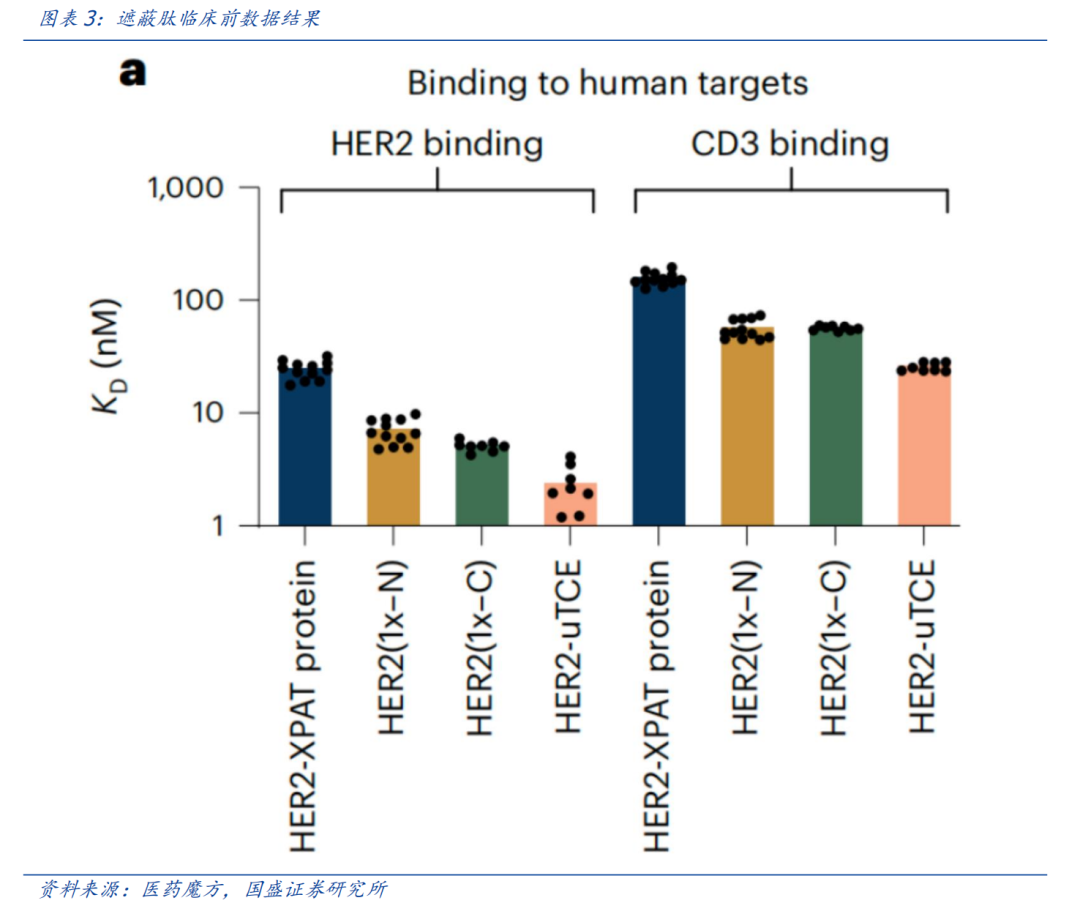
遮蔽的保护作用意味着剂量可以爬得更高。
2 Janux Thepertuics,Vir Biotechnology验证成功遮蔽肽技术可行性
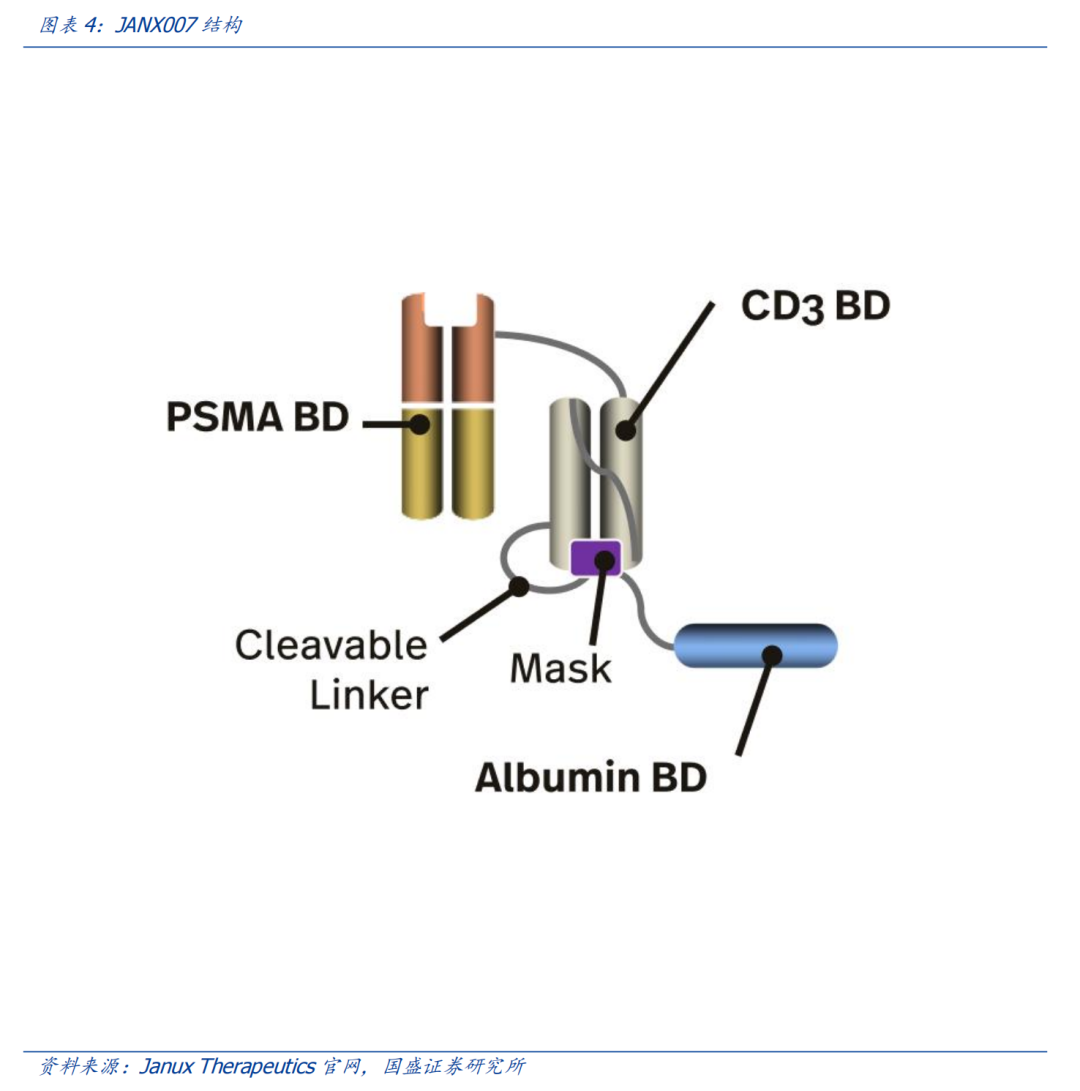
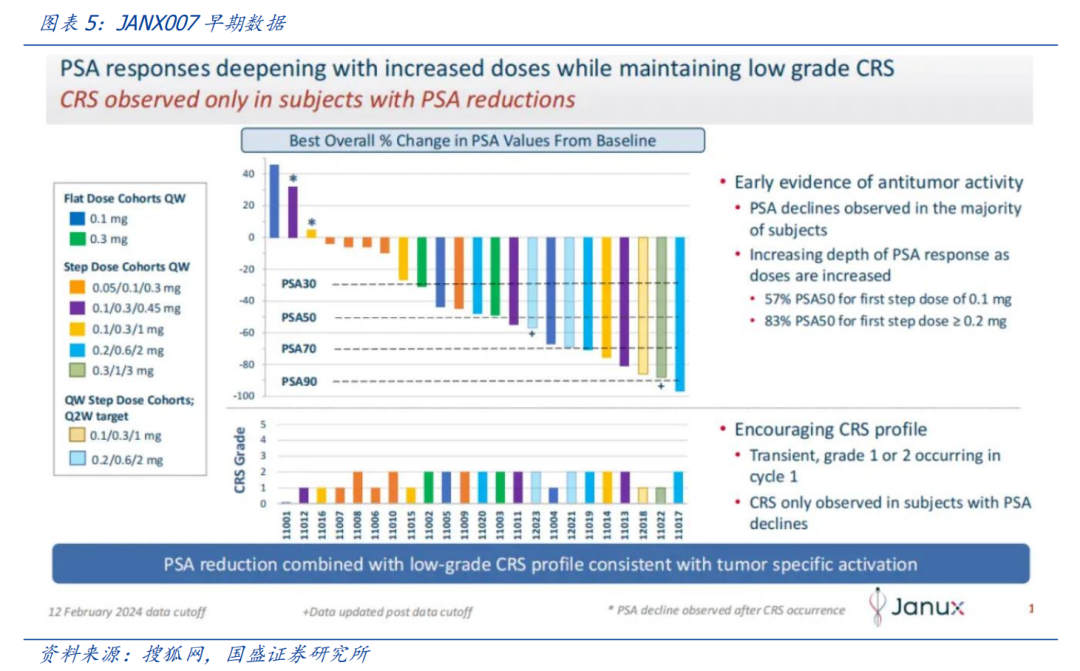
Janux最为领先的候选产品JANX007是一款靶向PSMA的TRACTr分子,旨在通过提供比传统TCE疗法更高浓度的活性药物,在mCRPC(转移性去势抵抗性前列腺癌)患者中产生强大的抗肿瘤活性,同时减少不良反应,目前正在进行1期临床试验,该研究在2022年下半年启动。
2024年2月26日,Janux Therapeutics宣布在正在进行的剂量递增试验中,针对mCRPC(转移性去势抵抗性前列腺癌)的JANX007和针对实体瘤的JANX008取得积极的安全性和有效性数据。消息公布次日,Janux股价暴涨229.47%,随后公司宣布公开发行普通股,以推进其内部产品管线的临床开发,并用于一般企业用途。
在起始剂量≥0.1 mg时,18名受试者中有14名(78%)实现了PSA30下降,18名受试者中有10名(56%)实现了PSA50下降。在起始剂量≥0.2 mg时,6名受试者中全部6名(100%)实现了PSA30下降,6名受试者中有5名(83%)实现了PSA50下降。JANX007≥0.2 mg的初始爬坡剂量推动了更深入、更持久的PSA反应,包括1名受试者实现了PSA90下降。
Vir Biotechnology在2025年1月公布旗下两款T细胞接合器(TCE)VIR-5818与VIR-5500的初步1期临床数据。数据显示,这两种在研疗法在曾接受过多线治疗的癌症患者中观察到早期临床应答的信号,剂量递增仍在进行中,最大耐受剂量(MTD)尚未确定。其中,VIR-5500在治疗前列腺癌患者的临床试验中让100%患者的前列腺特异性抗原(PSA)指标产生下降。这些初步结果为该公司从外部引进的PRO-XTEN平台提供了临床验证。
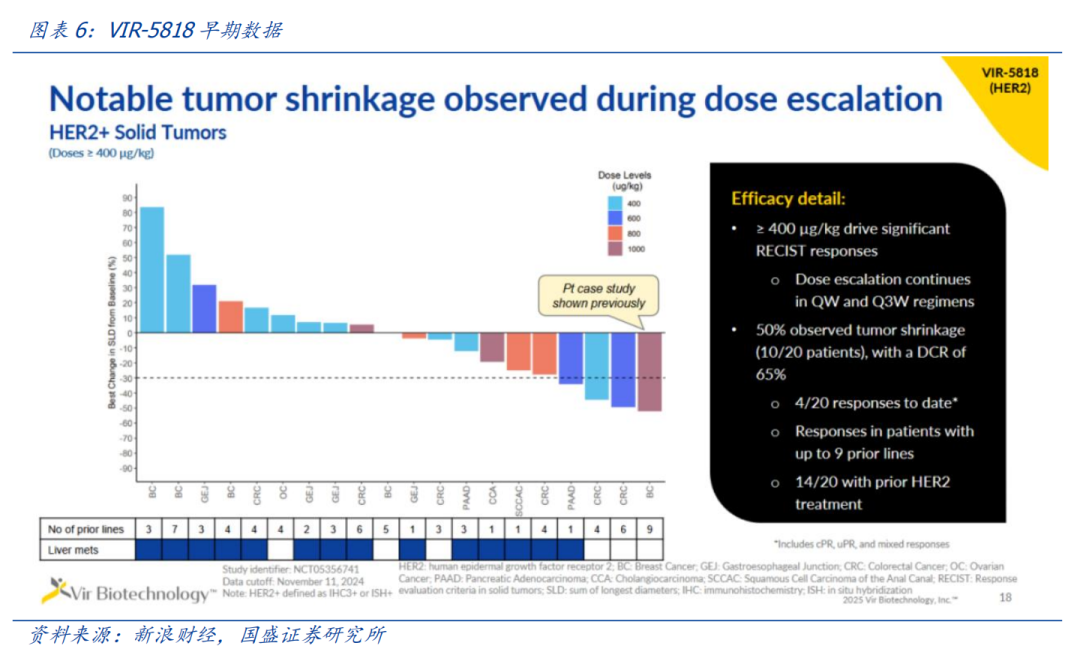
VIR-5818在一项1期临床试验中接受评估,旨在检视其作为单药的安全性和药代动力学,以及与帕博利珠单抗联合使用的效果。受试者包含多种HER2表达癌症的患者,包括乳腺癌和结直肠癌(CRC)。该试验已在单药治疗组中招募了79名接受过多线治疗的患者。
初步疗效数据显示,接受≥400 µg/kg VIR-5818的患者中,50%(10/20)出现剂量依赖性肿瘤缩小。其中一些患者此前已接受多达9种治疗方案。在HER2阳性CRC患者亚组中,观察到强效抗肿瘤活性,这些患者已用尽标准治疗手段。在该亚组中,33%(2/6)的患者在早期剂量下达到确认的部分缓解(cPR),其中一名患者在数据截止时持续cPR超过18个月。
3 国内公司积极布局,临床催化渐进
3.1 奥赛康:全球首个IL-15遮蔽肽前药分子
ASKG315是由奥赛康子公司AskGene自主研发的、拥有全球自主知识产权的SmartKine®细胞因子前药平台技术孵化的首个细胞因子类药物,该技术旨在避免系统水平的‘Cytokine Sink’,延长PK,并增加疾病组织的渗透和靶向性。
ASKG315是全球首个开展临床的IL-15前药分子,有望从根本上解决细胞因子治疗窗狭窄,无法广泛应用的临床痛点。
3.2 德琪医药:自助研发的空间位阻前药平台 AnTenGager
T细胞衔接器(TCE)已在血液系统肿瘤的治疗中显示良好疗效,并在近期开始显示出治疗实体瘤的潜力。但由于不理想的疗效和较高的CRS风险,TCE在实体瘤治疗中的应用仍非常有限。
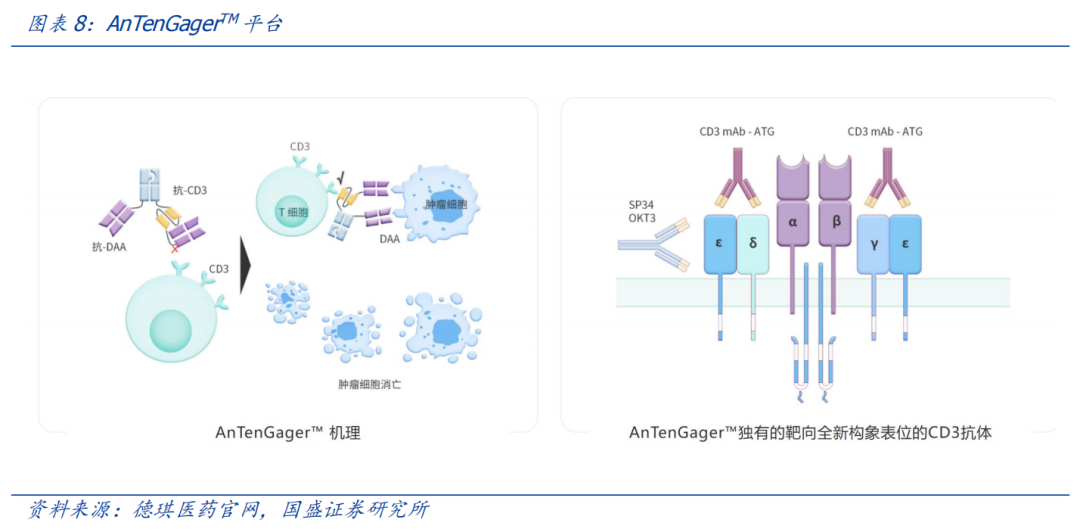
德琪医药的新型“2 1”TCE技术平台AnTenGager™可以有效克服这些问题,因为它可通过诱导疾病相关抗原(DAA)依赖的T细胞结合和激活,在实现较强的活性的同时降低发生CRS的风险。
它可实现与DAA(包括表达水平较低的DAA)的二价结合,同时使用了由德琪医药自主研发的可靶向作用于一个特殊构象表位的CD3抗体序列。它利用长度优化过的连接子将一个CD3单链抗体(scFv)结合至TAA抗体铰链区,这让起初被Fab抗体臂掩盖的CD3结合域仅在DAA交联条件下暴露,进而实现T细胞的条件性激活。
3.3 百济神州:启动 IL-15 前药联用替雷利珠单抗联治疗实体瘤临床
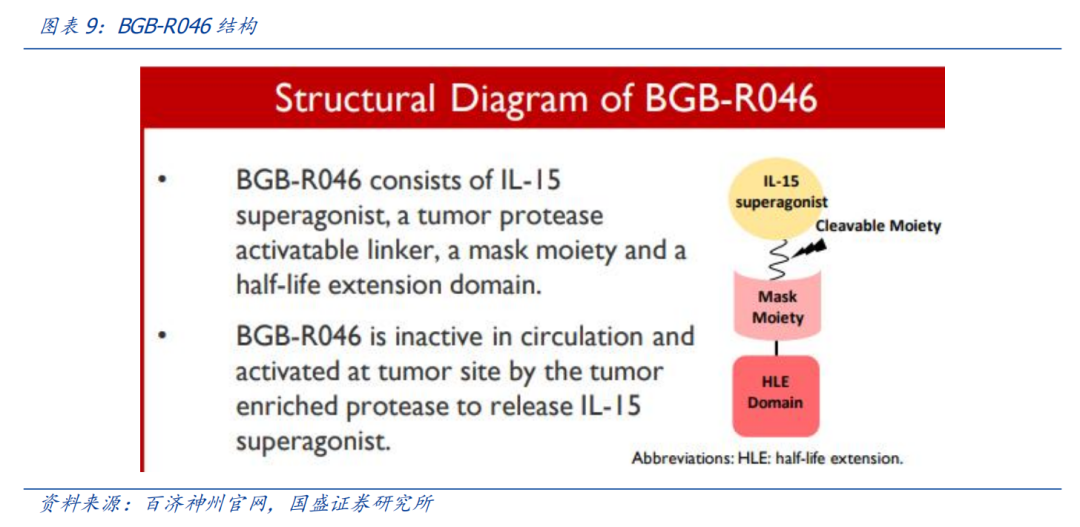
2024 年 6 月,百济神州针对实体瘤的新分子实体新药 BGB-R046 获批临床,拟开发治疗晚期或转移性实体瘤。这是一款细胞因子疗法,为该公司在泛肿瘤领域布局的一款 IL-15前体药物。
2024 年 4 月 22 日,生物技术公司 ImmunityBio 宣布,其开发的 IL-15 超级激动剂 N-803获得 FDA 批准上市(商品名:Anktiva),用于与卡介苗(BCG)联用治疗对卡介苗不响应且伴有原位癌的非肌层浸润性膀胱癌(NMIBC)成年患者,这些患者伴或不伴有乳头状瘤。N-803 成为全球首款获批上市的 IL-15 药物。
风险提示



 VIP复盘网
VIP复盘网
