对于癌症患者而言,找到适合自己的治疗药物,是实现精准抗癌的关键一步。但在临床实践和药物研发中,传统的肿瘤模型要么制备成本高、周期长,要么无法精准模拟人体肿瘤的生长环境,导致药物筛选结果与临床实际存在偏差,难以满足个体化诊疗的需求。器官芯片技术的出现为解决这一难题带来了曙光,却又因制备复杂、可扩展性差等问题难以落地。
近日,Adv Sci发表了一项重磅研究,成功研发出一款深度学习驱动的可规模化肿瘤器官芯片平台,一举突破了肿瘤药物筛选的多项技术瓶颈,让精准抗癌的药物匹配变得更高效、更贴合临床实际。

这款名为OC-Plex的肿瘤器官芯片平台,从根源上解决了传统平台的制备痛点。平台全程采用热塑性材料经注塑成型打造,实现了工业级的规模化、低成本生产,目前已有超7000台设备应用于相关研究,稳定性和实用性得到充分验证。依托专利的通道几何结构和表面处理技术,平台通过毛细管钉扎效应实现无屏障水凝胶限制,无需多孔膜、微柱等传统物理屏障,既简化了设计工艺,更能让细胞间实现直接相互作用,最大程度还原体内肿瘤的生长微环境。
同时,该平台具备极强的兼容性和可扩展性,不仅支持组织特异性细胞外基质培养,还能通过恒流、重力驱动等多种灌注模式实现细胞共培养,成像兼容性优异。4个基础版OC-Plex 8可组合为OC-Plex 32高通量版本,完美适配主流自动化成像系统,水凝胶填充成功率超90%,还能在灌注通道接种内皮细胞形成血管化小管,构建出更贴近体内生理状态的肿瘤微环境,为药物检测提供了更精准的模型基础。
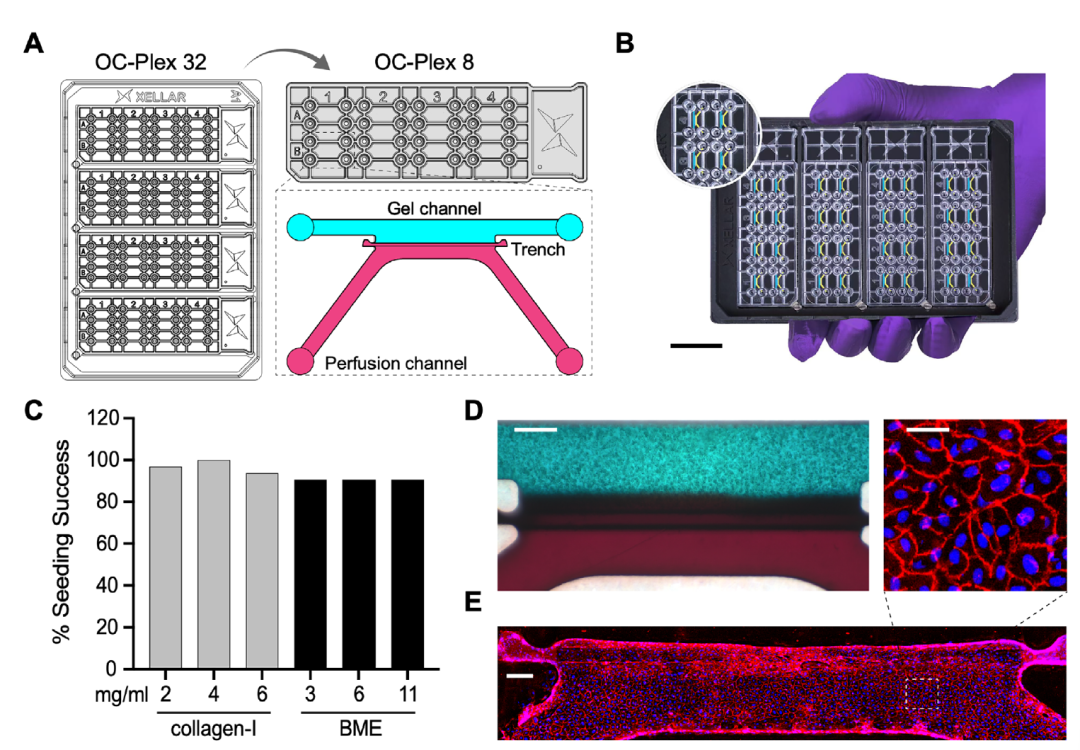 图1:OC-Plex平台的通道设计、实物及性能验证结果
图1:OC-Plex平台的通道设计、实物及性能验证结果
研究团队首先验证了OC-Plex对多种肿瘤细胞的生长支持能力,在胰腺导管腺癌、肺癌、结直肠癌等常见肿瘤细胞系的测试中,该芯片均能有效支持细胞生长、球形成型、细胞迁移,且在静态和动态灌注条件下均能维持细胞高活力,实现长达15天的稳定培养。同时,研究建立了基于成像的表型分析流程,对比传统的CellTiter-Glo ATP检测法,成像分析获得的标准化存活面积等指标,在量化药物效应时不仅能呈现一致的药物敏感性趋势,还具有更小的数据变异,检测的准确性和稳定性显著更优。
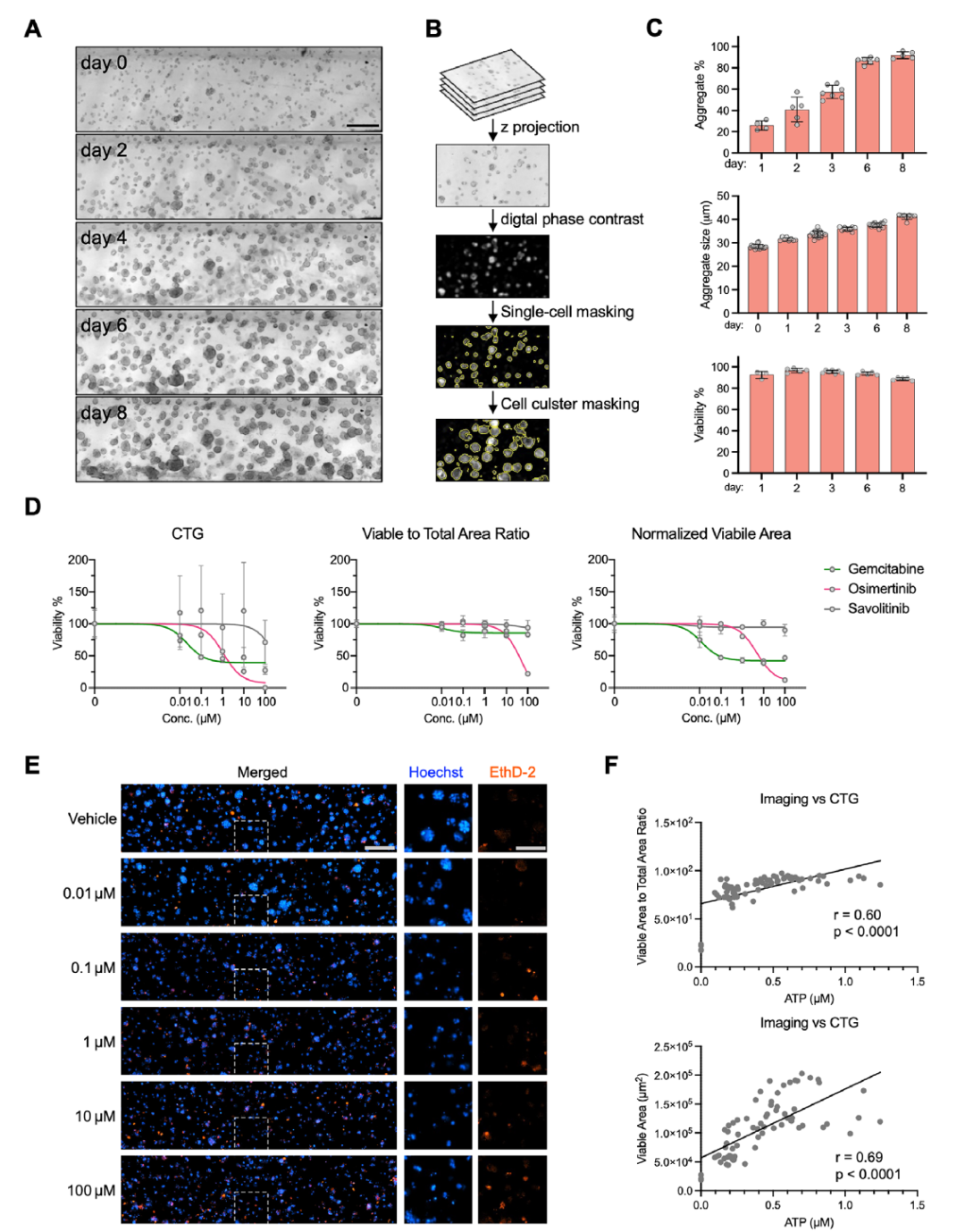 图2:OC-Plex芯片支持肿瘤细胞生长及药物敏感性检测的结果
图2:OC-Plex芯片支持肿瘤细胞生长及药物敏感性检测的结果
为进一步验证芯片的药物筛选效能,研究团队在胰腺、肺、结直肠肿瘤细胞系中,开展了短期和长期培养后的药物敏感性检测,并与传统2D培养模型对比。结果显示,芯片上长期培养的肿瘤细胞对药物的敏感性显著低于短期培养及2D模型,更贴近体内肿瘤的真实药物响应特征,直接证实2D模型易产生药物有效的假阳性结果,而OC-Plex能更真实地模拟体内肿瘤的药物反应。此外,该平台的自动化操作流程可将实验总操作时间减少约70%,大幅提升了药物筛选的效率,凸显了其高通量规模化应用的潜力。
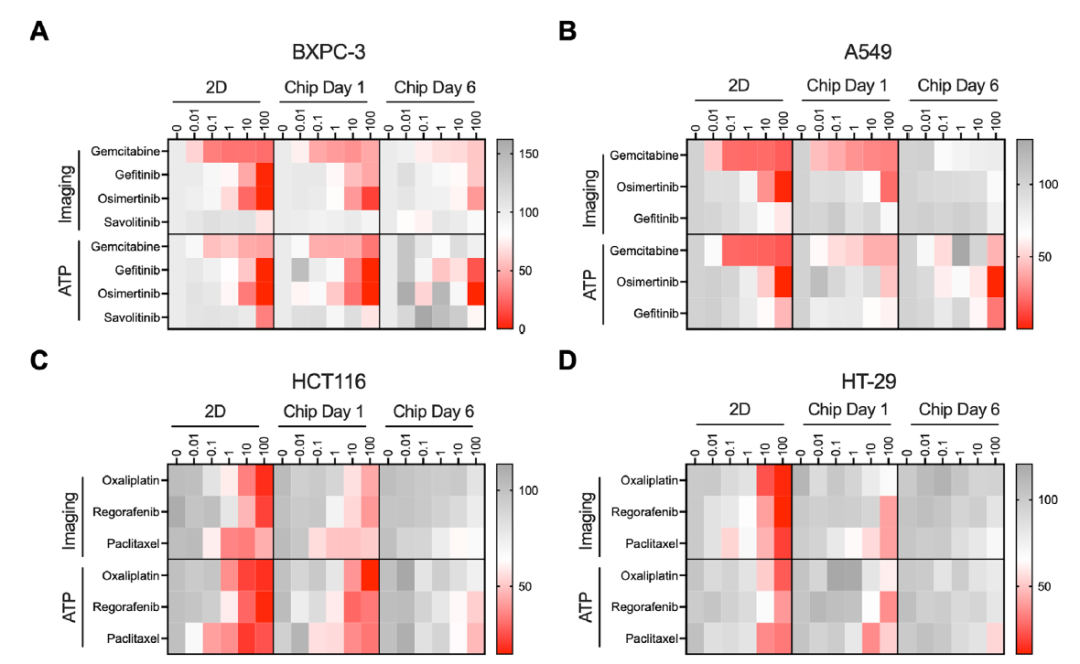 图3:不同肿瘤细胞系在2D培养和OC-Plex芯片模型中的药物敏感性热图
图3:不同肿瘤细胞系在2D培养和OC-Plex芯片模型中的药物敏感性热图
临床相关性是肿瘤药物筛选模型的核心价值,这也是OC-Plex最核心的亮点。在肺鳞癌患者源原代细胞的药物检测中,2D模型显示培美曲塞具有显著药效,而OC-Plex芯片的检测结果却显示该药物对患者源细胞无明显作用,这一结论与临床中肺鳞癌患者无法从培美曲塞治疗中获益的实际情况高度一致。不仅如此,该芯片还能支持患者源胃癌类器官与外周血单个核细胞的免疫-肿瘤共培养,在PD-1抑制剂信迪利单抗的检测中,可清晰呈现剂量和时间依赖性的抗肿瘤效应,实现对免疫检查点抑制剂活性的精准定量评估,证实其可用于临床相关免疫治疗方案的筛选,为免疫治疗药物的研发提供了全新工具。
为解决传统荧光染色操作繁琐、存在光毒性、易改变细胞行为且只能实现终点检测的问题,研究团队还为OC-Plex整合了基于U-net卷积神经网络的深度学习图像翻译模型,成功实现从明场图像到荧光染色图像的精准预测,皮尔逊相关系数达0.89-0.92,能有效提取荧光特异性信息。
这一深度学习模型实现了无标记、纵向的表型分析,可在药物处理的多个时间点生成荧光等效图像,开展动态的药物效应分析。其中基线归一化的活细胞检测指标,对药物剂量响应的检测灵敏度显著高于传统的终点荧光染色,还能有效解决3D培养中普遍存在的染色不均问题,为药物检测提供了更高效、更精准的分析方法,让研究人员能全程追踪细胞对药物的动态响应过程。
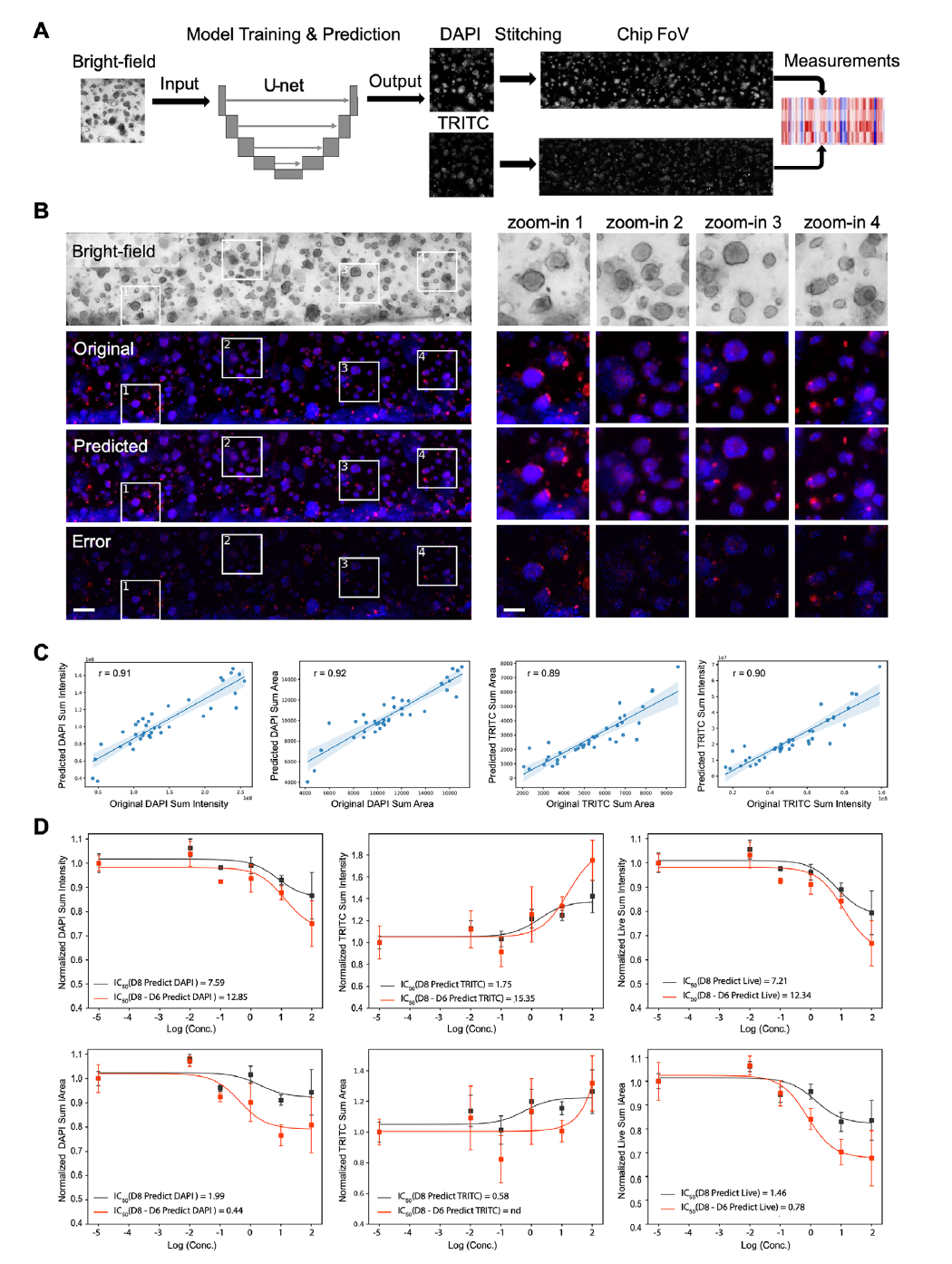 图4:深度学习赋能芯片上无标记成像分析以量化药物作用效果
图4:深度学习赋能芯片上无标记成像分析以量化药物作用效果
此次研发的OC-Plex肿瘤器官芯片平台,融合了工程学、生物学和人工智能分析的前沿技术,从设计、制备到功能实现,全方位突破了传统肿瘤药物筛选模型的技术瓶颈。全热塑性材质的选用让平台实现了规模化、低成本的工业级制备,专利结构设计精准模拟了体内肿瘤微环境;成像表型分析流程提升了药物检测的准确性,而深度学习模型的整合则实现了无标记、动态的药物效应监测,进一步提升了检测灵敏度。
更重要的是,该平台兼具高通量和患者特异性的双重优势,对患者源细胞的药物响应预测结果与临床高度契合,既可以用于临床肿瘤患者的个体化药物检测,为医生制定精准的治疗方案提供科学依据,也能助力抗肿瘤药物的临床前高通量筛选,大幅缩短新药研发周期、降低研发成本。
在癌症精准医疗的发展浪潮中,OC-Plex的研发成功为功能精准肿瘤学搭建了全新的技术框架,让肿瘤精准药物筛选从实验室走向临床应用成为现实。这一技术不仅突破了现有肿瘤药物筛选的诸多瓶颈,更有望推动癌症精准医疗向更高效、更贴合患者实际的方向发展,为广大肿瘤患者带来更具针对性的治疗方案,也为抗肿瘤药物的研发注入全新的技术动力,让每一位患者都能更快找到适合自己的抗癌药物,真正实现精准抗癌、高效抗癌。
参考文献:
Yuan YC, Xu B, McCormack J, et al. Deep Learning-Powered Scalable Cancer Organ Chip for Cancer Precision Medicine. Adv Sci (Weinh). Published online February 3, 2026. doi:10.1002/advs.202516660



 VIP复盘网
VIP复盘网
