IgE作为过敏反应和过敏性疾病治疗的核心靶点,市场潜力不容小觑。现阶段唯一获批的抗IgE抗体药物奥马珠单抗验证了其巨大临床价值。2025年,奥马珠单抗在美国市场给罗氏带来了30.75亿瑞郎(约合40亿美元、275亿人民币)的营收和32%的单产品年增长。2026年1月20日,GSK用22亿美元现金,持续印证着IgE作为黄金靶点的非凡潜力与广阔前景。
近日,在2026年美国过敏、哮喘和免疫学会年会(AAAAI 2026)上,天辰生物医药(苏州)股份有限公司(以下简称“天辰生物”)公布了其自主研发的全新一代抗IgE抗体LP-003在慢性自发性荨麻疹(CSU)适应症中,与奥马珠单抗头对头临床试验的顶线数据。研究显示,相较于奥马珠单抗,LP-003展现出全面的临床优势,在主要临床指标上均取得了优效的统计学结果,总体安全性与耐受性良好,展现了Best-in-Class的潜力。
该临床试验(CTR20233300,NCT06228560)为一项多中心、随机、双盲、安慰剂以及阳性药物(奥马珠单抗)对照的II期临床研究,旨在比较LP-003与奥马珠单抗及安慰剂组在治疗H1抗组胺控制不佳的慢性自发性荨麻疹患者的疗效。
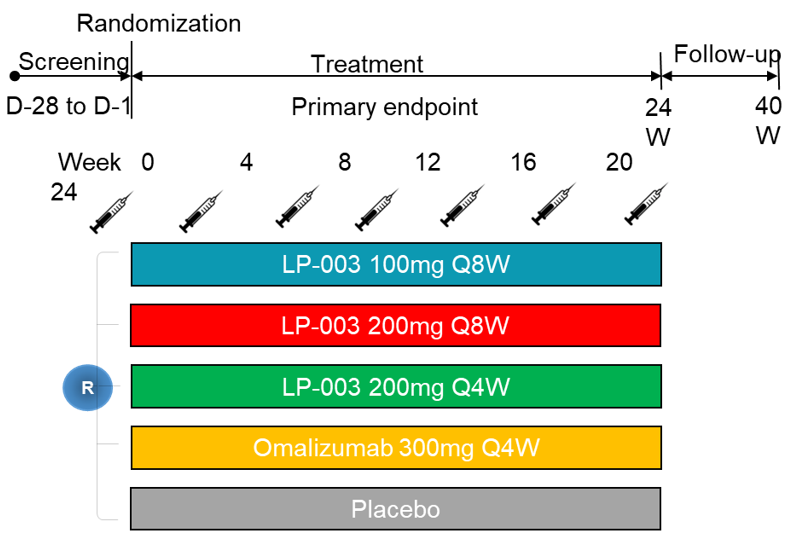
本项临床试验共入组202例患者,随机分配至LP-003三组(100 mg Q4W,200 mg Q4W,200 mg Q8W)、奥马珠单抗组(300 mg Q4W)以及安慰剂组,总疗程为24周。
在另一个关键指标“12周的UAS7较基线变化(UAS7 LS Mean Change from baseline at week 12)”上,LP-003 100 mg Q8W组、LP-003 200 mg Q8W组、LP-003 200 mg Q4W组,奥马珠单抗组和安慰剂组为别为-23.15、-26.63、-24.74、-21.85和-13.98。LP-003各组均显著优于安慰剂组,LP-003 200 mg组疗效优于奥马珠单抗组,且不同剂量组呈剂量依赖效应。其中,LP-003 200 mg Q8W组相比奥马珠单抗,在疗效上有显著的提升且具有统计学差异(p=0.0137)。
在治疗的第四周时,LP-003各个治疗组受试者荨麻疹症状完全缓解率为35~35.9%,早期即展现了优异的疗效,显著优于安慰剂组,也优于奥马珠单抗组。
本项 Ⅱ 期临床研究结果表明,LP‑003 在经抗组胺药治疗后症状仍未控制的慢性自发性荨麻疹患者中,初步展现出非常有潜力治疗效果,且整体呈现出良好的安全性特征,为后续临床研究的开展提供了重要依据。
关于天辰生物
天辰生物是一家处于临床阶段的创新生物制药研发企业,主要专注于过敏性疾病及自身免疫系统疾病的创新疗法开发。
核心产品LP-003是天辰生物自主研发的全新一代抗IgE抗体用于治疗各类过敏性疾病,包括过敏性鼻炎、慢性自发性荨麻疹、过敏性哮喘、慢性鼻窦炎伴鼻息肉和食物过敏等适应症。
目前,LP-003慢性自发性荨麻疹适应症的III期临床试验预计将于2026年上半年启动。季节性过敏性鼻炎适应症的III期临床试验已完成患者入组,预计将在2026年第三季度或之前向NMPA提交BLA,届时,LP-003将成为继奥马珠单抗获批上市20余年来,第一个也是唯一提交上市申请的新一代抗IgE抗体,这必将成为中国创新药发展历史上一个重要的里程碑



 VIP复盘网
VIP复盘网
