
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
百奥泰
688177 |
-1.22%
|
最新:30.69
开盘:31.19 昨收:31.07 |
开盘%:0.39%
振幅%:3.7% 换手%:1.63% |
最高:31.65
最低:30.5 量比:1.17 |
总市值:127 亿
流通值:127 亿 成交额:4 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
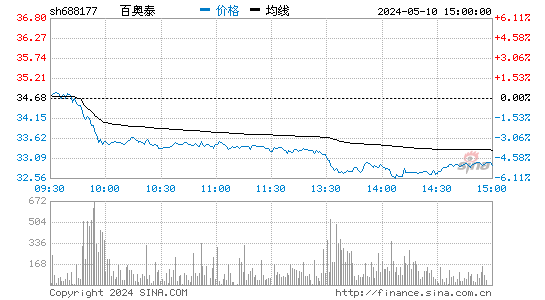
- 分时图
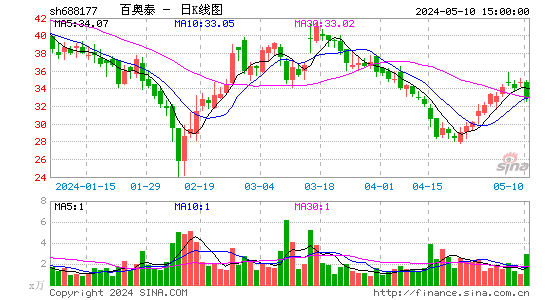
- 日K图
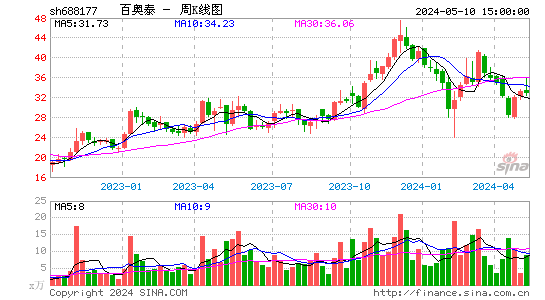
- 周K图
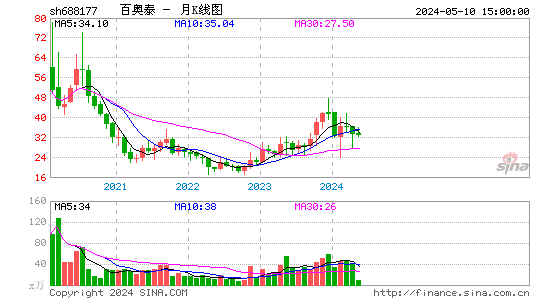
- 月K图
百奥泰:生物科技领域的股市新星
全面解析百奥泰股票及其公司概况
公司概况
百奥泰成立于XXXX年,总部位于中国,是一家拥有自主知识产权和核心竞争力的生物制药企业。公司自成立以来,始终秉承“创新驱动发展,科技造福人类”的理念,致力于研发和生产高质量的生物药品。
研发实力
在研发方面,百奥泰拥有一支由行业专家和资深科学家组成的研发团队。他们利用先进的生物技术和研发平台,针对肿瘤、自身免疫性疾病等重大疾病领域进行深入探索。
产品线
百奥泰的产品线涵盖了多个治疗领域,其中不乏具有自主知识产权的创新药。这些药物的研发和生产均遵循国际最高标准,确保了产品的安全性和有效性。
市场表现
作为上市公司,百奥泰的股票在资本市场中表现抢眼。随着公司业绩的稳步增长和研发实力的不断提升,其股价也呈现出稳步上升的态势。
社会责任
百奥泰在追求经济效益的同时,也积极履行社会责任。公司注重环保和可持续发展,积极参与公益事业,为社会和谐稳定贡献力量。
{summary}
总结:百奥泰作为一家专注于生物制药领域的上市公司,凭借强大的研发实力和丰富的产品线,在资本市场中展现出了强劲的增长潜力。同时,公司积极履行社会责任,为社会和谐稳定贡献力量。关键词:百奥泰、股票、生物科技、医药研发、创新药。{/summary}
2025-07-22 09:51
【创新药概念股反复活跃 成都先导、诚达药业双双涨超10%】7月22日电,成都先导、诚达药业双双涨超10%,百奥泰、赛升药业、丽珠集团、海特生物、辰欣药业、健康元等多股涨超5%。消息面上,国家医保局召开医保支持创新药械系列座谈会第一场,围绕“对创新药械开展医保综合价值评价”议题深入交流,提出意见建议。
2025-07-21 16:33
【百奥泰:BAT4406F注射液新增微小病变肾病/局灶节段性肾小球硬化适应症获临床试验批准】7月21日电,百奥泰(688177.SH)公告称,公司收到国家药品监督管理局核准签发的关于BAT4406F注射液新增微小病变肾病/局灶节段性肾小球硬化适应症的《药物临床试验批准通知书》。BAT4406F为公司开发的全人源抗CD20抗体,已获批临床试验的适应症包括视神经脊髓炎谱系疾病、微小病变肾病/局灶节段性肾小球硬化。
2025-06-23 16:57
【百奥泰:与SteinCares就BAT2406(度普利尤单抗)注射液签署授权许可及生产、供货和商业化协议】6月23日电,百奥泰(688177.SH)公告称,公司与SteinCares签署授权许可及生产、供货和商业化协议,将BAT2406(度普利尤单抗)注射液在巴西以及其余拉丁美洲地区市场的独占的产品商业化权益有偿许可给Stein,交易金额最高至1,000万美元,其中包括100万美元首付款、累计不超过900万美元里程碑付款,以及净销售额的两位数百分比作为收入分成。协议自生效日期起生效,十五年届满(初始期限),可自动延长两年(续签期限)。该协议的签订预计将对未来业绩产生积极影响,有利于提升公司的盈利能力。
2025-06-20 15:34
百奥泰:Usymro(乌司奴单抗注射液)获欧洲药品管理局人用药品委员会积极意见
2025-05-23 15:58
【百奥泰:BAT2206(乌司奴单抗)注射液获美国FDA上市批准】23日讯,百奥泰(688177.SH)公告称,公司收到美国FDA关于BAT2206(乌司奴单抗)注射液(美国商品名称:STARJEMZA)上市批准的通知。该药品适用于成人和儿童的中重度斑块状银屑病、活动性银屑病关节炎、中重度活动性克罗恩病和中重度活动性溃疡性结肠炎。百奥泰已在全球多区域开展该药品的商业化进程,并已向中国NMPA和欧洲EMA递交上市许可申请。
2025-05-22 17:04
【百奥泰:计划调整BAT3306(帕博利珠单抗)的开发策略,终止BAT3306正在开展的BAT3306-002研究】根据美国食品药品监督管理局(FDA)近期对生物类似物产品的技术沟通内容,以及欧盟药品管理局(EMA)于2025年4月发布的关于生物类似物审评的思考性文件,均体现出欧美药监官方在审批生物类似物产品的上市申请时,疗效比对研究的必要性已经大大下降,对于大多数生物类似物产品,疗效比对研究已经不是上市审批时需要提交的必要数据。经审慎考虑,公司认为目前正在开展的BAT3306-002研究对于BAT3306在欧美药监官方的上市审评已无必要,公司决定终止该研究。公司将持续与药品监督管理部门保持密切沟通,针对生物类似物审评的最新政策动态,公司将审慎评估并作出决策后决定未来是否继续推进BAT3306项目。截至2025年4月30日,公司BAT3306研发项目累计投入2.24亿元。按照相关会计准则和公司会计政策,该项目的全部研发支出已计入相应会计期间损益,不会对公司当期及以后年度业绩产生实质性影响。
2025-05-08 18:07
【百奥泰:公司正在加紧准备BAT8006临床项目 估计本月开始入组受试者】5月8日电,百奥泰(688177.SH)在投资者关系活动上表示,公司会努力争取BAT2206在今年下半年和明年初在主要市场(中美欧)获得批准上市。BAT5906首个III期适应症wAMD研究的揭盲时间在2025年的二季度末,DME临床在开展中,公司已有计划针对CNV和CRVO开展注册临床研究,正在筹备阶段。托珠单抗皮下的开发及托珠欧洲的合作都在推进中,公司会尽快推进已经批准的静脉给药在欧洲销售。公司正在加紧准备BAT8006临床项目,估计本月开始入组受试者。
2025-04-23 18:58
【百奥泰:股东新余启恒计划减持不超过2%股份】23日讯,百奥泰(688177.SH)公告称,股东新余启恒因投资项目退出及资金安排需要,计划通过集中竞价、大宗交易方式减持其持有的公司股份,合计不超过828.16万股(含本数),占公司总股本不超过2%。
2025-04-23 18:58
百奥泰:新余启恒拟减持不超过2%。
2025-04-21 15:42
百奥泰:注射用BAT7111获得药物临床试验批准通知书
2025-04-11 14:12
创新药概念震荡拉升,海思科午后涨停,股价创出历史新高,一品红涨超10%,科兴制药、阳光诺和、百奥泰、百济神州、翰宇药业等多股涨超5%
2025-04-08 19:21
【百奥泰:2024年净亏损5.1亿元】百奥泰发布2024年年度报告,报告期内,公司实现营业收入7.43亿元,同比增长5.44%;归属于上市公司股东的净利润亏损5.1亿元,上年同期亏损3.95亿元。
2025-04-02 10:03
【创新药概念延续强势 润都股份7天4板】4月2日电,润都股份走出7天4板,哈三联2连板,海创药业涨超10%,热景生物、百奥泰、凯因科技、新诺威、迈威生物、诺思格等跟涨。消息面上,信达证券认为,随着二季度的临近,医保谈判、医保丙类目录落地预期、多个重要肿瘤药临床会议等事件有望成为新一轮创新药行情的催化剂。
2025-04-02 09:51
创新药概念再度拉升,海创药业涨超10%,哈三联2连板,百奥泰、益方生物、迪哲医药、圣诺生物等跟涨。
2025-03-31 16:29
百奥泰:与Intas Pharmaceuticals Ltd.就BAT2506(戈利木单抗)注射液签署授权许可与商业化协议收到1890万美元首付款
2025-03-13 18:21
百奥泰:戈利木单抗注射液(BAT2506)上市许可申请获得受理
2025-03-13 14:45
【百奥泰“戈利木单抗”生物类似药申报上市 系国内首个】3月13日,国家药品监督管理局药品审评中心官网显示,百奥泰的戈利木单抗注射液的上市申请已获受理,该药是国内首个申报上市的戈利木单抗生物类似药。资料显示,戈利木单抗原研药为强生Simponi,系一种TNF-α单抗,目前该药已在我国获批类风湿性关节炎和强直性脊柱炎两项适应症。2024年,Simponi为强生带来了21.90亿美元收入。目前,国内仅百奥泰一家布局戈利木单抗生物类似药。(证券时报)
2025-02-10 16:24
百奥泰:与Intas Pharmaceuticals Ltd.就BAT2506(戈利木单抗)注射液签署授权许可与商业化协议议,将公司的BAT2506(戈利木单抗)注射液在美国市场的独占的产品商业化权益有偿许可给Intas,首付款及里程碑款总金额最高至1.645亿美元,以及净销售额的两位数百分比作为收入分成
2025-02-10 16:23
百奥泰:注射用BAT1006联合曲妥珠单抗及化疗治疗乳腺癌获得药物临床试验批准通知书。
2025-02-07 16:51
【百奥泰:司库奇尤单抗注射液上市许可申请获得受理】7日讯,百奥泰公告,公司在研药品司库奇尤单抗注射液(BAT2306)的药品上市许可申请已获得国家药监局受理。BAT2306是百奥泰根据中国NMPA、美国FDA、欧盟EMA生物类似药相关指导原则开发的,能够选择性结合细胞因子-白细胞介素17A(IL-17A)并抑制其与IL-17受体的相互作用。该产品经审评审批通过后可获发药品批准证书并可投入生产、销售,但审评审批的办结时间无法预估,因此本次获得药品上市许可申请受理通知书对公司近期业绩不会产生影响。
2025-02-07 16:50
百奥泰:司库奇尤单抗注射液(BAT2306)上市许可申请获得受理。
2025-01-24 16:29
【百奥泰:戈利木单抗注射液上市许可申请获欧洲EMA受理】24日讯,百奥泰公告,公司向欧洲药品管理局(EMA)递交了BAT 2506(戈利木单抗)注射液的生物制品上市申请,并于近日收到了欧洲EMA受理的通知。BAT 2506(戈利木单抗)注射液是百奥泰根据中国NMPA、美国FDA、欧洲EMA生物类似药相关指导原则开发的戈利木单抗生物类似药。该产品原研药为美国强生公司的Simponi®(欣普尼®),目前在全球范围内已有多个适应症获批。BAT 2506(戈利木单抗)注射液获得欧洲EMA上市申请受理后仍须经过一系列审评审批,审评周期及审评结果尚具有不确定性,本次上市申请的受理对公司近期业绩不会产生影响。
2025-01-24 16:28
百奥泰:BAT2506(戈利木单抗)注射液上市许可申请获得欧洲EMA受理
2024-12-16 17:35
百奥泰:与SteinCares签署授权许可及生产、供货和商业化协议,将公司的BAT2306(司库奇尤单抗)注射液在巴西以及其余拉丁美洲地区市场的独占的产品商业化权益有偿许可给Stein
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 未雨绸缪:多维度策略预防股票暴跌风险
- 股市智取反弹:精准布局的四大黄金法则
- 期权交易全解析:掌握金融衍生品的力量
- 短线炒股的艺术:技巧与风险控制并行
- 周五操盘法:实战短线的策略与要点解析
- 炒股智慧:为何不满仓,仓位控制的艺术
- 国债期货:金融衍生品的避险利器
- 股市风云:应对被套策略与心态调整
- 如何在重大技术位前精准判断与应对:策略与实践
- 双底形态的深度剖析与实战技巧
- 合理配置股票仓位:实现投资效益最大化的策略
- 揭秘股市:洞察主力吸筹的四大信号与策略
- 价值投资者的长期稳健收益之道
- 揭秘长牛庄股:技术分析与实战策略
- 尾盘布局,智取次日涨幅:深度解析尾盘埋伏选股策略
- 探索交易之路:老股民的交易心得与深刻体会
- 股市赚钱秘籍:七招助你大赚小赔
- 深度解析:如何精准捕捉龙头股见顶信号
- 炒股智慧:资深股民揭秘盈利与避坑法则
- 捕捉大牛股:揭秘市值视角下的投资秘诀
当前版本:V3.0

 VIP复盘网
VIP复盘网
