
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
长春高新
000661 |
0.59%
|
最新:102
开盘:101.4 昨收:101.4 |
开盘%:0%
振幅%:1.49% 换手%:1.51% |
最高:102.31
最低:100.8 量比:0.62 |
总市值:416 亿
流通值:408 亿 成交额:4 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
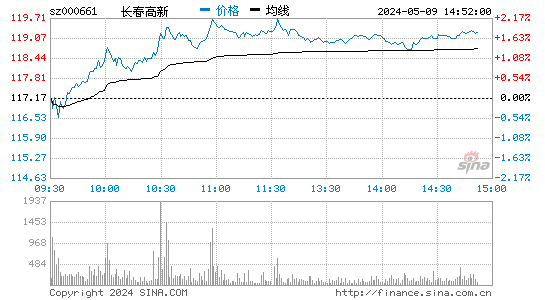
- 分时图
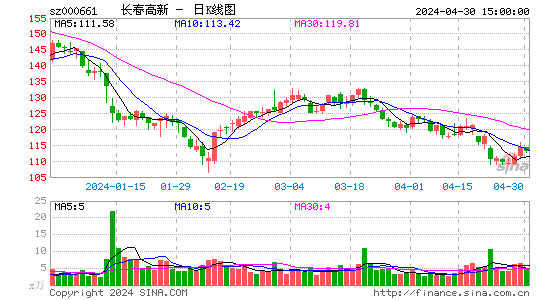
- 日K图
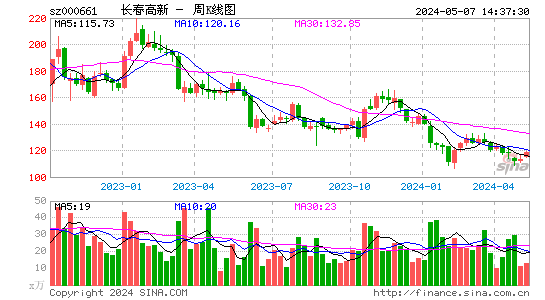
- 周K图
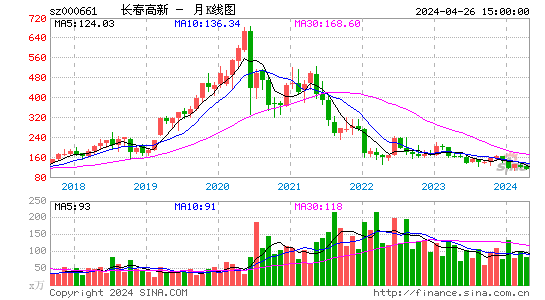
- 月K图
长春高新股票分析
深度解析长春高新股票及其市场表现
公司概况
长春高新是一家集生物制药、疫苗研发、高新技术产业于一体的综合性企业。公司成立于XXXX年,总部位于中国长春市,经过多年的发展,已成为国内生物制药领域的佼佼者。
业务领域
生物制药:长春高新在生物制药领域拥有强大的研发和生产能力,主要产品包括基因工程药物、生物类似药等。
疫苗研发:公司在疫苗研发方面也取得了显著成果,为国内外市场提供了高质量的疫苗产品。
财务表现
从近几年的财务数据来看,长春高新的营业收入和净利润均呈现出稳步增长的趋势。
市场前景
随着国内生物制药市场的不断扩大,长春高新有望凭借其在该领域的领先地位,进一步拓展市场份额。
总结
长春高新作为一家生物制药及高新技术产业公司,拥有强大的研发能力和市场竞争力。在财务表现方面,公司呈现出稳步增长的趋势。未来,随着市场的不断扩大,长春高新有望继续保持强劲的发展势头。
{summary}
长春高新是一家生物制药及高新技术产业公司,涉及生物制药、疫苗研发等多个领域。公司财务表现稳健,市场前景广阔,是投资者关注的热点股票之一。{/summary}
2025-07-07 13:44
创新药概念震荡回落,科兴制药跌超15%,荣昌生物、君实生物、贵州百灵、汇宇制药、长春高新等跌幅居前。
2025-07-03 13:03
【创新药概念持续走高 长春高新等多股涨停】7月3日电,午后创新药概念持续走高,长春高新封涨停,此前神州细胞、九芝堂、华海药业、未名医药涨停,赛升药业、热景生物、微芯生物、迈威生物、广生堂涨超7%。消息面上,国家医保局、国家卫生健康委印发《支持创新药高质量发展的若干措施》,其中提到,支持创新药进入基本医保药品目录和商业健康保险创新药品目录;增设商业健康保险创新药品目录。
2025-07-03 09:41
【创新药概念股反复活跃 塞力医疗3连板】7月3日电,塞力医疗3连板,神州细胞、微芯生物、赛升药业、长春高新、未名医药涨超5%,华海药业、佐力药业、热景生物等跟涨。消息面上,近日国家医保局、国家卫生健康委联合印发《支持创新药高质量发展的若干措施》,提出5方面16条措施,强调对创新药研发、准入、入院使用和多元支付进行全链条支持。
2025-07-03 09:38
【创新药概念股延续强势,塞力医疗3连板】创新药概念股延续强势,塞力医疗3连板,九芝堂、微芯生物、长春高新、未名医药、佐力药业等跟涨。
2025-07-02 20:55
长春高新:子公司注射用伏欣奇拜单抗在境内获批上市。
2025-07-01 21:36
【公告精选:比亚迪上半年销量约214.6万辆同比增长33%;长春高新、欣旺达筹划发行H股】7月1日电,【热点】长春高新:拟发行H股并在香港联交所上市。欣旺达:拟发行H股并在香港联交所上市。安井食品:H股发行价格为每股60港元,7月4日上市交易。新大陆:设立境外子公司并取得美国MSB牌照,推进跨境支付业务的拓展。爱建集团:目前公司未开展稳定币相关业务。百川股份:公司实控人、董事长郑铁江被留置。*ST元成:涉嫌年报等财务数据虚假披露,遭证监会立案。杭州高新:控股股东将变更为巨融伟业,7月2日复牌。上纬新材:控股股东筹划控制权变更,7月2日起停牌。苏州规划:筹划购买东进航科控股权,7月2日起停牌。海南华铁:拟公开发行不超20亿元公司债券。【经营业绩】国脉科技:上半年净利润同比预增60.52%—100.33%。孩子王:上半年净利润同比预增50%—100%。新和成:上半年净利润同比预增50%—70%。石大胜华:上半年预亏5200万元到6000万元。上汽集团:上半年整车销量205.26万辆,同比增长12.35%。比亚迪:上半年新能源汽车销量约214.6万辆,同比增长33.04%。北汽蓝谷:子公司上半年销量67152辆,同比增长139.73%。千里科技:上半年汽车整车销量38728辆,同比增长61.62%。长城汽车:上半年汽车销量56.98万台,同比增长1.81%。吉利汽车:6月汽车总销量23.6万部,同比增长42%。赛力斯:6月新能源汽车销量46086辆,同比增长4.44%。东安动力:6月发动机销量同比增长82.79%。【增减持】越秀资本:控股子公司广州资产拟增持越秀地产港股股票。龙迅股份:股东及董监高拟合计减持公司不超2%股份。复洁环保:隽洁投资拟减持公司不超3%股份。无锡振华:无锡康盛拟减持公司不超1%股份。【中标合同】国芯科技:中标4600万元汽车电子芯片项目。模塑科技:获外饰件产品项目定点,预计总销售额12.36亿元。常铝股份:全资子公司签订1.65亿元总承包合同。威胜信息:中标2749.72万元南方电网招标项目。华菱线缆:近期电力新能源领域中标金额4.56亿元。福龙马:6月预中标环卫服务项目总额1.81亿元。浦东建设:子公司中标多个重大项目,金额总计19.64亿元。江河集团:控股子公司中标雄安国贸中心酒店精装修项目,金额约1.88亿元。【其他】仙鹤股份:拟110亿元投建竹浆纸用一体化高性能纸基新材料项目。永茂泰:拟约4.5亿元投建墨西哥汽车零部件智能制造基地。航天长峰:拟挂牌转让航天柏克55.45%股权,减少损失。动力新科:全资子公司上汽红岩被申请破产重整。
2025-07-01 17:42
长春高新:授权公司管理层启动公司境外发行股份(H股)并在香港联合交易所有限公司上市相关筹备工作
2025-06-19 21:44
【长春高新:子公司流感病毒裂解疫苗(BK-01佐剂)临床试验申请获批】长春高新晚间公告,公司子公司长春百克生物科技股份公司收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,百克生物流感病毒裂解疫苗(BK-01佐剂)临床试验申请获得批准。本次百克生物获批临床的流感病毒裂解疫苗(BK-01佐剂)接种对象为60岁及以上人群,接种后可刺激机体产生更强的免疫应答,用于预防流感病毒引发的流行性感冒。
2025-06-19 20:48
【公告精选:圣诺生物上半年净利预增253.54%至332.1%;台基股份实控人拟变更为湖北省国资委】6月19日电,【经营数据】圣诺生物:上半年预计净利润同比增加253.54%至332.1%顺丰控股:5月速运物流业务收入同比增长13.36%圆通速递:5月快递产品收入58.49亿元 同比增长14.85%韵达股份:5月快递服务业务收入同比增长6.75%申通快递:5月快递服务业务收入同比增长13.01%【热点】二连板时代出版:公司对京东科技的间接持股比例极低 不涉及稳定币业务三连板诺德股份:公司股票换手率急剧放大,远超前期正常水平二连板中京电子:近期生产经营情况正常 无未披露重大事项金种子酒澄清:公司经营范围不存在变更主业情况 未来仍将做优做强白酒主业联建光电:公司经营情况、内外部经营环境未发生重大变化楚天龙:控股股东之一致行动人在股票交易异动期间共减持公司股份119.01万股山东黄金:控股子公司山金国际拟发行H股并在香港联交所上市康达新材:拟以现金方式收购中科华微不低于51%的股权【再融资】信达证券:向专业投资者发行不超100亿元公司债券的注册申请获许可国投资本:向专业投资者发行不超40亿元可续期公司债券注册申请获许可【股权变动】台基股份:公司实控人拟变更为湖北省国资委 股票复牌线上线下:控股股东筹划公司控制权变更 股票停牌【增减持、回购】腾讯控股:6月19日回购100万股股份 耗资约5亿港元千红制药:实控人的一致行动人已增持公司股份960万股 拟继续增持【中标合同】北京科锐:近日中标及预估中标多个项目 金额合计约1.54亿元三星医疗:全资子公司预计合计中标1.43亿元国家电网采购项目建工修复:联合承接3276万元土壤污染源头综合治理EPC项目万达信息:拟签订中国人寿新一代人力资源管理系统二期项目合同【重大投资】中国建筑:下属子公司投资上海市宝山区房地产开发项目宁波远洋:拟使用不超20亿元投资建造4艘4300TEU集装箱船恒润股份:拟投资12亿元建设年产2000套风电齿轮箱零部件项目迪威尔:拟投资3.058亿元建设深海承压零部件产品精密制造项目中信国安:拟以股权出资形式增资中国广电湖南公司汇通能源:子公司拟出资3000万元参投基金【其他】厦门钨业:5000吨(首期)高性能钕铁硼磁性材料项目投产星辉娱乐:球员转会直接贡献公司税后净利润1975.61万欧元宁德时代:拟使用不超过45亿元闲置募集资金进行现金管理ST智知:全资子公司收到627万元政府补助天康生物:控股子公司天康制药北交所上市辅导验收完成赛升药业:与华大蛋白签订新药技术转让合同日发精机:意大利MCM公司申请破产众生药业:RAY1225注射液用于肥胖/超重的III期临床试验完成首例参与者入组盘龙药业:获得中国合格评定国家认可委员会(CNAS)实验室认可证书长春高新:子公司流感病毒裂解疫苗(BK-01佐剂)临床试验申请获批健康元:JKN2301干混悬剂药物临床试验获批百克生物:流感病毒裂解疫苗临床试验申请获批新华制药:OAB-14干混悬剂完成Ⅱ期临床中国首例患者入组
2025-06-19 19:11
【长春高新:子公司百克生物流感病毒裂解疫苗(BK-01佐剂)临床试验申请获得批准】6月19日电,长春高新(000661.SZ)公告称,公司子公司百克生物收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,百克生物流感病毒裂解疫苗(BK-01佐剂)临床试验申请获得批准。
2025-06-13 19:43
【长春高新:子公司两款药品临床试验申请获批】6月13日电,长春高新(000661)6月13日晚间公告,子公司金赛药业收到国家药监局核准签发的两份《药物临床试验批准通知书》,授权经销合作产品醋酸甲地孕酮口服混悬液(美适亚®)的境外生产药品注册临床试验申请获得批准;GenSci134注射液的境内生产药品注册临床试验申请获得批准。
2025-06-13 19:18
长春高新:醋酸甲地孕酮口服混悬液(美适亚)药物临床试验申请获得批准
2025-06-12 13:15
创新药概念午后拉升,奥赛康涨停,博瑞医药、睿智医药涨超10%,海思科、长春高新、微芯生物、舒泰神等涨幅居前
2025-06-12 13:09
【生物制品板块异动拉升,派林生物涨停】生物制品板块异动拉升,派林生物涨停,荣昌生物、长春高新、君实生物、百普赛斯、诺诚健华等跟涨。
2025-06-04 13:35
【医美概念震荡走高 水羊股份涨超17%】6月4日电,医美概念震荡走高,水羊股份涨超17%,九芝堂、*ST金比涨停,福瑞达、长春高新、朗姿股份等涨幅居前。
2025-05-28 17:48
【长春高新:子公司GenSci128片新药临床试验申请获得美国FDA批准】5月28日电,长春高新(000661.SZ)公告称,公司子公司金赛药业收到美国FDA关于同意GenSci128片开展临床试验的批准。GenSci128片是针对TP53 Y220C突变的选择型重激活剂,用于治疗携带TP53 Y220C突变的局部晚期或转移性实体瘤。该药物已在中国获批开展临床试验。如临床试验申请进展顺利,将有利于公司拓宽业务结构,优化产品结构,并丰富完善战略领域产品线布局、提升公司核心竞争力。
2025-04-28 16:56
长春高新:伏欣奇拜单抗注射液临床试验申请获得批准
2025-04-20 15:44
长春高新:一季度净利润4.7亿元,同比下降44.95%
2025-04-20 15:41
【长春高新:一季度净利润同比下降44.95%】4月20日电,长春高新(000661.SZ)发布2025年第一季度报告,公司实现营业收入29.97亿元,同比下降5.66%;归属于上市公司股东的净利润为4.73亿元,同比下降44.95%。主要原因是公司销售业务相关人员数量增长导致费用增加,以及研发投入持续增长。
2025-04-14 21:02
【长春高新:公司暂无对美国出口产品相关业务】长春高新4月14日在互动平台表示,公司目前暂无对美国出口产品相关业务,后续公司将持续关注国内国际经贸政策和环境变化。
2025-03-20 16:17
长春高新:子公司GenSci120注射液新药临床试验申请获得美国食品药品监督管理局默示许可
2025-03-19 13:54
【长春高新等投资成立生物科技新公司】企查查APP显示,近日,上海赛鹜健飞生物科技有限公司成立,法定代表人为刘灏,经营范围包含:工业酶制剂研发;生物化工产品技术研发;专用化学产品销售等。企查查股权穿透显示,该公司由长春高新旗下长春金赛药业有限责任公司等共同持股。
2025-03-04 17:08
长春高新:子公司聚乙二醇重组人生长激素注射液增加国内同品种已批准适应症补充申请获得国家药监局批准。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 震荡市中的涨停秘籍:操盘手的实战智慧
- 揭秘涨停多方炮:精准捕捉介入时机的策略分析
- 揭秘短线选股真谛:以人气为导向的智慧策略
- 期权基础解析:深入探索行权操作的奥秘
- 探秘基金重仓股:如何把握投资机会
- 股市智慧:掌握平衡,稳健前行
- KDJ指标深度解析:掌握短线交易的艺术
- 揭秘:长线投资需谨慎,六类股票慎入陷阱
- 情绪与板块题材:股市波动的双引擎
- 深入解析止跌现象:逻辑、判断与应对策略
- 短线炒股智慧:精准把握卖出时机
- 个股增量资金入驻的盘面迹象深度剖析
- 股民智慧:探索股市生存的七大法则
- 揭秘股东人数背后的投资迷局:洞悉数据背后的真相
- 揭秘股市牛股洗盘策略:洞悉主力动向,精准捕捉机遇
- 应规避不操作的股票以防被套
- 揭秘短线牛股精选策略:技术面与消息面的双重奏
- 揭秘股市资金流向与大单操作:DDX识别技巧深度剖析
- 你真的会使用周K线吗?深度解析周K线的应用与实战策略
- 便宜之道:深度剖析价值投资的精髓与误区
当前版本:V3.0

 VIP复盘网
VIP复盘网
